- Bei einem Aszites sammelt sich Flüssigkeit in der Bauchhöhle an.
- Wasser im Bauch kann eine Folge einer Krebserkrankung sein. Dann sprechen Fachleute von einem malignen Aszites.
- Wir erklären, wie eine Punktion die Beschwerden lindern kann und informieren über weitere Maßnahmen und Therapien bei malignem Aszites.
Informationen zu malignem Aszites bei Krebserkrankten
Dieser Text bietet keine Informationen zu Aszites als Komplikation nach Operationen oder bei Leberzirrhose.
Wichtig: Informationen aus dem Internet können Ihnen einen Überblick bieten. Sie sind aber nicht dazu geeignet, die Beratung durch einen Arzt oder eine Ärztin zu ersetzen.
Aszites durch Krebs: Wichtiges in Kürze
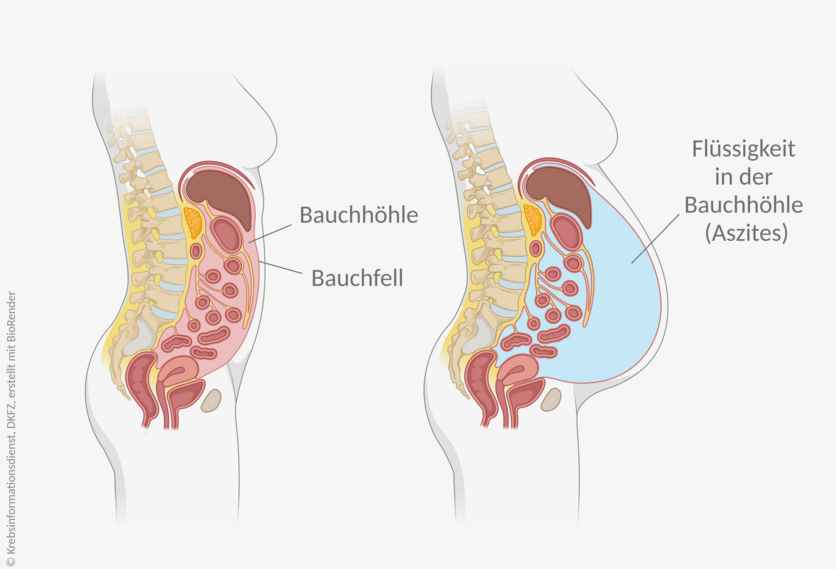
Bild: © Krebsinformationsdienst, DKFZ; erstellt mit BioRender.com
Bei einem Aszites sammelt sich Flüssigkeit in der Bauchhöhle an. Das kann verschiedene Ursachen haben.
Bei einem malignen Aszites ist eine Krebserkrankung die Ursache für das Wasser im Bauch.
Meist verursachen Metastasen im Bauchfell oder in der Leber einen malignen Aszites. Dieser kann aber auch durch Bauchfellkrebs (Peritonealkarzinom) entstehen.
Bei für einen Aszites typischen Beschwerden untersuchen Ärztinnen und Ärzte den Bauch mit verschiedenen Methoden:
- Sie tasten den Bauch ab und achten auf typische Anzeichen für einen Aszites.
- Mit Ultraschall können sie Flüssigkeit im Bauchraum sichtbar machen.
- Bei einer Punktion entnehmen sie etwas von der Aszitesflüssigkeit. Fachleute untersuchen die Eigenschaften der Flüssigkeit im Labor mit besonderen Methoden.
Die Behandlung bei einem malignen Aszites richtet sich nach der individuellen Erkrankungssituation der Patientin oder des Patienten.
Bei den meisten Erkrankten tritt ein Aszites im fortgeschrittenen Stadium einer Krebserkrankung auf. Eine Heilung ist oft nicht mehr möglich.
Ziel der Maßnahmen ist es dann:
- Die Flüssigkeitsmenge im Bauchraum zu verringern, um die dadurch entstehenden Beschwerden zu lindern.
- Komplikationen wie beispielsweise eine Bauchfellentzündung zu vermeiden.
Eine Operation oder Chemotherapie ist nur für wenige Patientinnen und Patienten mit malignem Aszites eine geeignete Behandlungsmöglichkeit.
Fragen Sie Ihre Ärztinnen und Ärzte
Welche Maßnahmen und Therapien in Ihrer individuellen Erkrankungssituation möglich sind, erfahren Sie von ihrem behandelnden Fachpersonal.
Symptome bei Aszites

Bild: © Maya23K, iStock
Viele Erkrankte bemerken zunächst nicht, dass sich Flüssigkeit im Bauchraum ansammelt. Oder sie vermuten andere Ursachen. Bei manchen entdecken eine Ärztin oder ein Arzt das Bauchwasser zufällig bei einer Ultraschalluntersuchung des Bauches.
Erst wenn sich 1 bis 2 Liter Flüssigkeit im Bauch angesammelt haben, treten bei den meisten Betroffenen erste, oft unspezifische Beschwerden auf.
Dazu gehören beispielsweise:
- unangenehmes Druckgefühl oder Schmerzen im Bauch
- schnelles Sättigungsgefühl und Appetitlosigkeit
- Verdauungsbeschwerden wie zum Beispiel Verstopfung oder Blähungen
- Übelkeit und Erbrechen
- Schluckauf
- Sodbrennen
Wenn sich im Bauchraum viel Flüssigkeit ansammelt, kann das folgende Beschwerden verursachen:
- Der Bauch wird dick und wölbt sich nach außen. Außerdem fühlt er sich hart an.
- Der Bauchnabel wölbt sich nach außen.
- Der vergrößerte Bauchumfang kann die Beweglichkeit einschränken und die Atmung erschweren.
- Die Flüssigkeit im Bauch kann dazu führen, dass man ungewollt zunimmt.
- Die Verdauungsbeschwerden können zu einer Mangelernährung und Gewichtsverlust führen.
- Fehlen dem Körper Eiweiße, nehmen auch die Muskeln ab. Betroffene können sich dann nur noch eingeschränkt bewegen.
- Erkrankte sind schnell müde und erschöpft (Fatigue).
- Bei manchen Kranken kommt es zu einem Nabel- oder Leistenbruch.
- Die Flüssigkeit kann sich auch im Gewebe der Beine oder im Genitalbereich sammeln (Ödeme).
Wichtig zu wissen
Eine seltene, aber sehr gefährliche Komplikation bei einem Aszites ist eine Infektion des Bauchfells mit Bakterien, eine sogenannte Bauchfellentzündung. Erkrankte mit einem Aszites sollten bei plötzlich auftretenden, heftigen Bauchschmerzen oder hohem Fieber schnellstmöglich in eine Arztpraxis oder Klinik gehen.
Untersuchungen: Ursachen abklären
Verdacht auf Aszites: Ansprechpartner finden
Hilfreiche Informationen finden Sie in unserem Text "Krebsärzte, Krebskliniken: Wie findet man Spezialisten?" und in unserem Informationsblatt "Arzt- und Kliniksuche" (PDF).
Bei typischen Beschwerden eines Aszites führen Ärztinnen und Ärzte verschiedene Untersuchungen durch. Ihr Ziel ist es, den Aszites nachzuweisen. Sie suchen aber auch nach der Ursache des Aszites: Je mehr Informationen dem behandelnden Ärzteteam vorliegen, desto besser kann es die Maßnahmen und die Behandlung auf die individuelle Erkrankungssituation anpassen.
Anamnese und körperliche Untersuchung: Beschwerden und Symptome erfassen
Bild: © Pressmaster, Shutterstock.com
In einem Gespräch beschreiben die erkrankte Person, Angehörige oder Pflegende, welche Beschwerden wann und wo auftreten.
Im Anschluss untersucht die Ärztin oder der Arzt den Bauch der Patientin oder des Patienten:
- Sie klopfen auf den Bauch und beurteilen das dabei entstehende Geräusch, den sogenannten Klopfschall.
- Ist bereits viel Wasser in der Bauchhöhle, können sie eine Wellenbewegung der Flüssigkeit ertasten.
- Sie erfassen den Bauchumfang.
- Sie untersuchen den Bauch auf weitere, für einen Aszites typische Anzeichen, wie zum Beispiel gespannte Haut, sichtbare Venen oder ein nach außen gestülpter Bauchnabel.
Ultraschall
Mit einem Ultraschall des Bauches können Ärztinnen und Ärzte Flüssigkeitsansammlungen im Bauchraum sichtbar machen. Dabei können sie sehr geringe Mengen Bauchwasser entdecken – auch wenn diese noch keine oder nur geringe Beschwerden verursachen.
Punktion
Bei einem neu aufgetretenen Aszites untersuchen Ärzte die Aszitesflüssigkeit, um möglichst genaue Informationen über die Ursachen des Aszites zu gewinnen. Dafür entnehmen sie mit einer Punktion etwas Flüssigkeit aus der Bauchhöhle.
So läuft die Punktion ab: Die erkrankte Person legt sich mit leicht erhöhtem Oberkörper hin. Die Ärztin oder der Arzt desinfiziert die Haut am Bauch und betäubt den Bereich um die Einstichstelle. Dann führen sie eine Hohlnadel durch die Bauchdecke in die Bauchhöhle. Dabei kontrollieren sie die Position der Nadel mit Hilfe von Ultraschall. Ist die Nadelspitze in dem mit Flüssigkeit gefüllten Bereich positioniert, entnimmt die Ärztin oder der Arzt mehrere Proben für eine Laboruntersuchung.
Wichtig zu wissen
Hat sich bereits eine große Flüssigkeitsmenge angesammelt, kann die Ärztin oder der Arzt nach der Probenentnahme die Flüssigkeit ableiten (Parazentese).
Für Patientinnen und Patienten ist die Punktion in der Regel wenig körperlich belastend. Bei den meisten Erkrankten kann die Punktion ambulant durchgeführt werden. Möglicherweise kann aber auch ein kurzer stationärer Aufenthalt sinnvoll sein, beispielweise bei einem schlechten körperlichen Allgemeinzustand oder mehreren Begleiterkrankungen.
Nur bei wenigen Betroffenen treten die folgenden möglichen Nebenwirkungen auf:
- Blutergüsse und/oder kurzzeitige Blutungen an der Einstichstelle
- Infektionen der Wunde oder des Bauchraums. Bei einer bakteriellen Infektion müssen Betroffene möglicherweise Antibiotika einnehmen.
- Verletzungen der inneren Organe oder Strukturen. Diese sind möglich, kommen aber nur selten vor.
Wichtig zu wissen
Eine Bauchfellentzündung (Peritonitis) ist eine häufig auftretende Komplikation bei Aszites. Eine Peritonitis muss auch ohne Nachweis von Bakterien mit Antibiotika behandelt werden.
Zytologie
Im Labor untersuchen Fachleute die entnommene Flüssigkeit mit zytologischen Methoden. Die Ergebnisse liefern wichtige Informationen über die Ursache des Aszites.
Unter anderem untersuchen Fachleute die in der Aszitesflüssigkeit enthaltenen Zellen:
- Bakterien sind ein Hinweis auf eine Bauchfellentzündung.
- Tumorzellen in der Flüssigkeit sind ein sicherer Nachweis für einen malignen Aszites. Sind keine Tumorzellen nachweisbar, ist ein maligner Aszites jedoch noch nicht ausgeschlossen. Dann sind weitere Untersuchungen notwendig.
Weitere Untersuchungsmethoden
Bei den meisten Erkrankten reichen die Informationen aus der zytologischen Untersuchung des Bauchwassers für eine gesicherte Diagnose aus.
Ob bei einer Patientin oder einem Patienten weitere Untersuchungen nötig sind, entscheiden Ärztinnen und Ärzte abhängig von der individuellen Erkrankungssituation und von bereits vorliegenden Befunden.
Ist ein Aszites das erste Symptom einer Krebserkrankung, so suchen die Ärzte eventuell nach dem Primärtumor. Möglich sind dann beispielsweise eine Bauchspiegelung oder eine Spiegelung von Magen oder Darm, jeweils mit der Entnahme von Gewebeproben (Biopsie).
Sie haben Fragen zu Ihrem zytologischen Befund?
Unsere Ärztinnen und Ärzte beantworten kostenlos Ihre individuellen Fragen zu Ihren Untersuchungsergebnissen.
So erreichen Sie uns:
- am Telefon kostenlos unter 0800 420 30 40, täglich von 8 bis 20 Uhr
- über ein datensicheres Kontaktformular oder per E-Mail an krebsinformationsdienst@dkfz.de
Beschwerden lindern
Bei den meisten Erkrankten ist ein maligner Aszites eine Folge einer weit fortgeschrittenen Krebserkrankung.
Das behandelnde Ärzteteam und die Pflegenden versuchen
- die Beschwerden zu lindern,
- die Lebensqualität zu erhalten und
- Komplikationen zu vermeiden.
Sie wägen sorgfältig ab, welche Maßnahmen in der individuellen Erkrankungssituation möglich sind und welche Behandlungsmöglichkeiten die Patientin oder den Patienten zu stark belasten könnten.
Durch den Aszites verursachte akute Beschwerden verbessern sich schnell, wenn die Flüssigkeitsmenge im Bauchraum abnimmt. Es gibt verschiedene Möglichkeiten, das Wasser im Bauch zu verringern.
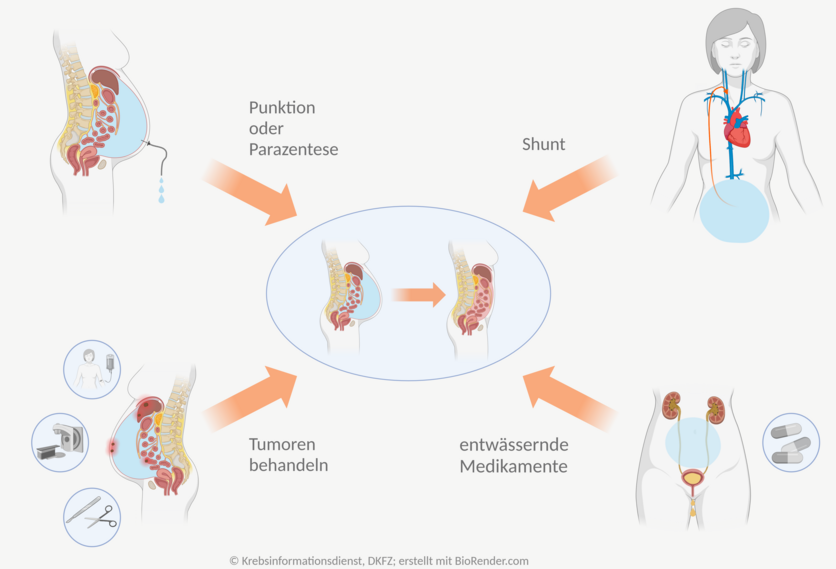
Bild: © Krebsinformationsdienst, DKFZ; erstellt mit BioRender.com
Parazentese: Punktion und Drainage
Lexikon
Parazentese: Fachleute durchtrennen oder durchstechen eine Körperstruktur – beispielsweise das Bauchfell oder das Trommelfell – um Flüssigkeit oder Gas nach außen abzulassen.
Punktion: Die Körperstruktur wird mit einer Hohlnadel durchstochen. Durch die Nadel kann Flüssigkeit entnommen werden.
Drainage: Die Flüssigkeit wird abgeleitet.
Bei einer Parazentese durchstechen eine Ärztin oder ein Arzt die Bauchdecke und lassen die Flüssigkeit nach außen ablaufen. Dies ist die schnellste und einfachste Möglichkeit, die durch den Aszites verursachten Beschwerden zu lindern.
Eine Parazentese kann in den meisten Erkrankungssituationen durchgeführt werden. Wie die Punktion zur Probenentnahme findet eine Parazentese bei den meisten Patientinnen und Patienten ambulant statt.
Wichtig zu wissen
Eine Parazentese kann regelmäßig wiederholt werden. Wann die nächste Parazentese nötig ist, hängt davon ab, wie schnell sich neue Flüssigkeit im Bauchraum ansammelt.
So läuft eine Parazentese ab: Eine Ärztin oder ein Arzt macht eine Punktion und führt eine Hohlnadel in den mit Flüssigkeit gefüllten Bauchraum ein. Anschließend kann die Flüssigkeit über die Hohlnadel ablaufen.
Das Fachpersonal kann auch einen kleinen Schlauch durch die Hohlnadel einführen oder einen Schlauch an die Nadel anschließen. Über den Schlauch kann die Flüssigkeit in einen Beutel oder eine Flasche ablaufen. Fachleute sprechen dann von einer Drainage.
Die meisten Patientinnen und Patienten haben nach einer Parazentese keine Kreislaufprobleme – auch nicht wenn mehrere Liter Flüssigkeit abgelassen werden. Weitere mögliche Nebenwirkungen einer Parazentese sind die gleichen wie bei einer Punktion.
Nur in bestimmten Erkrankungssituationen sind bei einer Parazentese zusätzliche Maßnahmen nötig:
- Blutverdünner absetzen: Bei einer Punktion kann die Einstichstelle bluten. Ob Erkrankte vor dem Eingriff blutverdünnende Medikamente absetzen sollten, hängt vom Wirkstoff und davon ab, wie dringend eine Punktion nötig ist.
- Transfusion von Blutplättchen: Nur Patienten mit sehr wenig Blutplättchen brauchen möglicherweise eine Transfusion von Blutplättchen. Das beugt starken Blutungen durch die Punktion vor.
- Transfusion von Bluteiweißen: Wenn Ärztinnen und Ärzte sehr viel Flüssigkeit ablassen, geben sie den Patienten manchmal Bluteiweiße. Das stabilisiert den Kreislauf. Ein Beispiel für ein solches Bluteiweiß ist Albumin.
Verweilkatheter
Für Patienten und deren Angehörige kann es sehr belastend sein, wenn die Parazentese häufig wiederholt werden muss und zu Krankenhausaufenthalten oder Infektionen führt. Manchmal können Dauerdrainagen wie beispielsweise ein Verweilkatheter die Lebensqualität deutlich verbessern.
Ein Verweilkatheter ist ein Plastikschlauch, der dauerhaft im Bauch bleibt. Am äußeren Schlauchende befindet sich ein Ventil. Damit können die erkrankte Person selber oder Pflegende die Flüssigkeit zu Hause ablassen.
Ärztinnen oder Ärzte können den Schlauch bei den meisten Betroffenen ambulant unter örtlicher Betäubung verlegen. Manchmal erhält die Patientin oder der Patient auch eine kurze Vollnarkose. Die möglichen Nebenwirkungen sind wie bei einer Punktion.
Shunts
Lexikon
Shunt: Eine natürliche oder operativ angelegte Verbindung zwischen zwei Blutgefäßen oder Hohlräumen, die normalerweise nicht verbunden sind
Bei einem Shunt legen Ärztinnen oder Ärzte eine künstliche Verbindung zwischen zwei Hohlräumen oder Blutgefäßen an. Bei einem Aszites kann durch einen Shunt die Flüssigkeit aus der Bauchhöhle dauerhaft abgeleitet werden. Ärzte können beispielsweise den Bauchraum durch einen Shunt mit einer Vene verbinden. Dann kann die Flüssigkeit aus der Bauchhöhle über das Blutgefäß ablaufen und muss nicht nach außen abgelassen werden.
Shunts können die Lebensqualität stark verbessern, da belastende wiederholte Parazentesen oder regelmäßiges Ablassen der Flüssigkeit durch einen Verweilkatheter entfallen.
Wichtig zu wissen
Shunts kommen nur für wenige Patientinnen und Patienten infrage. Erkrankte erfahren von ihrem behandelnden Ärzteteam, ob ein Shunt in ihrer individuellen Krankheitssituation möglich ist.
Die Shunt-Anlage ist aufwendiger als eine Parazentese: Ärztinnen und Ärzte verlegen einen Shunt durch eine Operation unter Vollnarkose. Die möglichen Nebenwirkungen entsprechen denen einer Operation.
Eine mögliche Komplikation eines Shunts ist eine bakterielle Infektion beim Anlegen. Außerdem können die Shunts verstopfen – dann ist eine erneute Operation notwendig.
Diuretika
Entwässernde Medikamente – sogenannte Diuretika, umgangssprachlich auch Entwässerungstabletten genannt – regulieren, wie viel Salz und Wasser die Nieren ausscheiden. Scheidet der Körper mehr Wasser aus, kann sich auch die Flüssigkeitsmenge im Bauchraum verringern.
Entsteht der Aszites dadurch, dass Lebermetastasen einen hohen Druck in der Pfortader verursachen, können Diuretika die Flüssigkeitsmenge im Bauch verringern. Das ist wissenschaftlich belegt.
Patientinnen und Patienten nehmen Diuretika zu Hause regelmäßig als Tabletten ein.
Mögliche Nebenwirkungen von Diuretika sind:
- Herzrhythmusstörungen
- gestörte Nierenfunktion
- niedriger Blutdruck
- Übelkeit und Erbrechen
- Mundtrockenheit und Durst
- Müdigkeit oder Muskelschwäche
Wichtig zu wissen
Patientinnen und Patienten sollten die Dosierung von Medikamenten nur nach Rücksprache mit den behandelnden Ärzten ändern.
Die Nebenwirkungen sind abhängig von der Dosierung. Starke Nebenwirkungen bessern sich meistens, wenn der oder die Betroffene eine geringere Dosis einnimmt.
Ein Therapieversuch mit Diuretika ist unabhängig von der Aszitesursache möglich.
Wissenschaftlich belegt ist die Wirksamkeit von Diuretika nur, wenn Lebermetastasen zu einem erhöhten Druck in der Pfortader und dadurch zu einem malignen Aszites führen.
Aber auch bei anderen Ursachen für den Aszites können Patientinnen und Patienten ausprobieren, ob Diuretika ihre Beschwerden verbessern.
Komplikationen behandeln: Bauchfellentzündung bei Aszites
Wichtig zu wissen
Eine Bauchfellentzündung ist eine gefährliche Komplikation. Sie muss mit Antibiotikum behandelt werden.
Eine Entzündung des Bauchfells, die durch Bakterien verursacht wird, ist eine gefährliche Komplikation bei einem malignen Aszites. Fachleute bezeichnen sie als spontane bakterielle Peritonitis (SBP).
Auslöser der Entzündung sind Darmbakterien. Sie können durch die veränderten Druckverhältnisse aus dem Darm in den Bauchraum gelangen und eine Infektion auslösen. Bakterien können aber auch durch eine Punktion oder bei einer Operation in den Bauchraum geraten.
Die Krankheitszeichen bei einer Bauchfellentzündung sind sehr unterschiedlich:
- Typische Anzeichen sind ein gespannter Bauch, Bauchschmerzen und Fieber.
- Bei manchen Erkrankten verschlechtern sich die Funktion von Leber, Niere und Gehirn.
- Andere haben keine oder nur unspezifische Beschwerden.
So wird eine Bauchfellentzündung behandelt: Patientinnen und Patienten müssen ein Antibiotikum einnehmen, um die bakterielle Infektion zu behandeln. Ärztinnen und Ärzte entnehmen vor Behandlungsbeginn oft durch eine Punktion etwas Bauchwasser und untersuchen, welche Bakterienarten die Entzündung verursachen. Dann können sie ein Antibiotikum geben, das gezielt gegen diese Bakterien wirkt. Aber auch wenn keine Bakterien nachweisbar sind, müssen Betroffene vorsichtshalber ein Antibiotikum einnehmen.
Ursachen behandeln
Da bei einem malignen Aszites Krebs die Ursache für das Wasser im Bauch ist, versuchen Ärzte, den Tumor zu verkleinern oder das Krebswachstum zu verlangsamen. Ziel der Behandlung ist, die Lebensqualität und die Lebenserwartung zu verbessern. Eine Heilung ist nur bei wenigen Patientinnen und Patienten möglich.
Es gibt verschiedene Behandlungsmöglichkeiten. Welche Therapien bei einer Patientin oder einem Patienten möglich sind, hängt von der individuellen Krankheitssituation ab.
Das behandelnde Ärzteteam berücksichtigt zum Beispiel
- die Ursache des Aszites: Je nachdem, ob der Aszites durch Krebszellen im Bauchfell oder in der Leber verursacht wird, gibt es unterschiedliche Therapiemöglichkeiten.
- die Eigenschaften der Krebszellen: Bei den meisten Erkrankten verursachen Metastasen den malignen Aszites. Die Behandlung von Metastasen richtet sich nach den Eigenschaften des Ausgangstumors. Davon hängt zum Beispiel ab, welche Chemotherapie geeignet ist.
- bereits durchgeführte Therapien: Behandlungsmethoden, die beim Ursprungstumor nicht wirksam waren, helfen mit hoher Wahrscheinlichkeit auch bei Bauchfellmetastasen nicht. Sie kommen daher nicht infrage.
- den körperlichen Allgemeinzustand und das Krankheitsstadium: Bei einer weit fortgeschrittenen Krebserkrankung oder einem schlechten körperlichen Allgemeinzustand können manche Therapien für die Betroffenen zu belastend sein. Die behandelnden Ärztinnen und Ärzte können daher nicht mehr alle Behandlungsmöglichkeiten anwenden.
Sprechen Sie mit Ihrem Behandlungsteam
Welche Therapien in Ihrer individuellen Erkrankungssituation möglich sind, erfahren Sie von Ihren behandelnden Ärztinnen und Ärzten. Diese informieren Sie auch, ob Sie an einer klinischen Studie teilnehmen können.
Metastasen im Bauchfell: Operation und Chemotherapie
Eine häufige Ursache für einen Aszites sind Metastasen im Bauchfell. Bei einem guten körperlichen Allgemeinzustand der der Patientin oder des Patienten, behandeln Ärzte die Metastasen mit einer Kombination aus Operation und Chemotherapie.
Wichtig zu wissen
Bauchfellmetastasen haben oft die gleichen Eigenschaften wie der Ursprungstumor. Bei Metastasen verwenden Ärztinnen und Ärzte daher meistens Therapien, die gegen den Ursprungstumor wirken.
Mehr Informationen zu den organspezifischen Behandlungsmöglichkeiten bieten unsere Texte zu den einzelnen Krebsarten.
Zum Weiterlesen
Mehr Informationen zum Ablauf und Nebenwirkungen bietet unser Text Operation (OP): Chirurgie bei Krebs
Operation: Ärztinnen und Ärzte versuchen, die von Krebszellen befallenen Bereiche des Bauchfells mit einer Operation möglichst vollständig zu entfernen. Sind weitere Organe im Bauchraum betroffen, entfernen sie diese soweit möglich ebenfalls.
Die Operation ist ein großer chirurgischer Eingriff. Patientinnen und Patienten bleiben dafür stationär im Krankenhaus.
Chemotherapie: Nach der Operation erhalten Erkrankte eine Chemotherapie. Diese zielt darauf ab, verbliebene Tumorreste zu behandeln.
Je nach individueller Erkrankungssituation kann die Chemotherapie als lokale Therapie in der Bauchhöhle durchgeführt werden. Dabei wird das Medikament im Anschluss an die Operation über einen Schlauch direkt in die Bauchhöhle geleitet. Es gelangt dadurch besser an die Tumore. Fachleute sprechen von einer intraperitonealen Chemotherapie.
Eine verbesserte Wirksamkeit dieser lokalen Chemotherapie beobachten Fachleute, wenn sie die verwendete Chemotherapielösung erhitzen. Bei einer solchen hyperthermen intraperitonealen Chemotherapie (HIPEC) spült die Ärztin oder der Arzt den Bauchraum direkt nach der OP für 30 bis 120 Minuten mit einer 41 bis 43 Grad Celsius warmen Chemotherapielösung.
Eine HIPEC ist nur für wenige Patientinnen und Patienten geeignet.
Fachleute erforschen in Studien, bei welchen Tumorarten und in welchen Situationen eine HIPEC wirksam ist.
Ob eine Patientin oder ein Patient für eine HIPEC geeignet ist, entscheiden Ärzte abhängig von der individuellen Erkrankungssituation.
Zum Weiterlesen
Informationen über die Nebenwirkungen von Chemotherapien bietet unser Text Chemotherapie-Medikamente: Wirkstoffe und Nebenwirkungen.
Zusätzlich bekommen Betroffene eine systemische Chemotherapie. Dabei erhalten sie die Medikamente über einen längeren Zeitraum und in regelmäßigen Abständen als Infusion oder als Tabletten.
Eine systemische Chemotherapie können Patientinnen und Patienten auch ambulant machen. Für die lokale Chemotherapie ist dagegen ein stationärer Aufenthalt nötig.
Was kann man bei einer weit fortgeschrittenen Erkrankung oder schlechtem körperlichen Allgemeinzustand tun? Auch dann kann eine Operation notwendig sein. Oft ist es aber nicht möglich, alle von Krebs betroffenen Bereiche vollständig zu entfernen. Dann ist das Ziel, den Aszites zu verringern und weitere Beschwerden wie beispielsweise Verdauungsprobleme zu verbessern.
Ist eine Operation nicht mehr möglich, können Patientinnen oder Patienten eventuell eine systemische Chemotherapie erhalten. Auch eine Bestrahlung kann in Frage kommen, falls diese beim Ursprungstumor wirksam war.
Weitere Behandlungsmöglichkeiten
Aktuell gibt es keine zugelassenen zielgerichteten Therapien gegen malignen Aszites.
Neue Therapiemöglichkeiten erforschen Fachleute in klinischen Studien. Ob Patientinnen und Patienten an einer Studie teilnehmen können, erfahren sie von ihrem behandelnden Ärzteteam.
Primärtumoren des Bauchfells
Primäre Bauchfelltumoren sind selten. Sie sind keine Metastasen, sondern entstehen aus Zellen des Bauchfells (Peritoneum).
Die Behandlung von primären Bauchfellkrebs ähnelt aber der Behandlung von Metastasen. Fachleute empfehlen eine Kombination aus Operation, HIPEC und systemischer Chemotherapie.
Lebermetastasen und Leberzellkrebs
Auch Leberzellkrebs oder Metastasen in der Leber können einen Aszites verursachen. Informationen zu den Behandlungsmöglichkeiten bieten unsere Texte zu Lebermetastasen und Leberzellkrebs.
Entsteht der Aszites, weil Lebermetastasen den Druck in der Pfortader erhöhen? Dann können Ärztinnen und Ärzte das Blut mit einem Shunt umleiten. Dadurch umgeht das Blut die Leber, der Druck nimmt ab und es wird weniger Flüssigkeit in den Bauchraum gedrückt. Fachleute bezeichnen diese spezielle Form eines Shunts als "transjugulären intrahepatischen portosystemischen Shunt". (TIPS). Ein TIPS kommt aber nur in seltenen Erkrankungssituationen in Frage.
Fragen Sie uns!
Sie haben Fragen, welche Behandlungsmöglichkeiten in Ihrer Erkrankungssituation in Frage kommen? Unsere Ärztinnen und Ärzte helfen Ihnen gerne kostenfrei weiter
- am Telefon täglich von 8 bis 20 Uhr unter 0800 420 30 40
- über ein datensicheres Kontaktformular oder per E-Mail an krebsinformationsdienst@dkfz.de
Leben mit Aszites: Mit der Belastung umgehen
Bei den meisten Erkrankten mit malignem Aszites ist der Krebs schon weit fortgeschritten. Eine Heilung ist nur noch selten möglich.
Ein Aszites kann das Wohlbefinden stark beinträchtigen. Die Erkrankung selbst, aber auch die Therapie können sehr anstrengend sein, beispielsweise regelmäßige Parazentesen in kurzen Abständen.
Deshalb versuchen Ärzte und Pflegende in der letzten Lebensphase dafür zu sorgen, dass es den Betroffenen bessergeht und keine Komplikationen auftreten. Dabei berücksichtigen sie die Bedürfnisse und Wünsche der Patientin oder des Patienten.
Was können Erkrankte und Angehörige selber tun?

Bild: © cheche22, iStock
Angehörige und Freunde können viel dazu beitragen, die Lebensqualität der erkrankten Person zu verbessern – auch im Endstadium der Krebserkrankung. Zum Beispiel kennen sie deren Vorlieben und Wünsche.
Auch die folgenden Tipps können Betroffenen und ihren Angehörigen helfen, das Wohlbefinden zu verbessern:
- Beobachten Sie die Flüssigkeitsmenge im Bauch. Eine Punktion kann normalerweise mit einem geringen zeitlichen Abstand wiederholt werden. Wenn die Beschwerden schlimmer werden, sprechen Sie mit dem Behandlungsteam, wann eine nächste Punktion möglich ist.
- Wenn Sie wenig Appetit haben oder schnell satt sind, können Sie Mahlzeiten beispielsweise mit Sahne, Butter, Öl, Zucker oder Honig anreichern. Das vermeidet einen Nährstoffmangel. Bei Bedarf können Sie sich an das Pflegepersonal oder das behandelnde Ärzteteam und an Ernährungsberater wenden. Sie beraten, wie Sie mit kalorien- und eiweißreicher Kost oder ergänzender Trinknahrung auch mit kleinen Portionen ausreichend Nährstoffe zu sich zu nehmen können.
- Salzen Sie Speisen nach Belieben. Wenn Sie nicht wissen, ob Sie in Ihrer individuellen Krankheitssituation beim Kochen auf Salz verzichten sollten, fragen Sie Ihr Behandlungsteam.
- Auch beim Trinken gilt: Nehmen Sie so viel Flüssigkeit zu sich, wie Sie möchten und brauchen. Wenn Sie weniger trinken sollen, informiert Sie Ihre behandelnde Ärztin oder Ihr behandelnder Arzt darüber.
Wichtig zu wissen
Auf Salz und Flüssigkeit zu verzichten, kann die Lebensqualität verringern. Sprechen Sie mit den behandelnden Ärztinnen und Ärzten, ob es stattdessen möglich ist, den Wasser- und Salzhaushalt mit Medikamenten zu regulieren.
Wer unterstützt Sie, mit den Belastungen durch den Aszites umzugehen?
Erkrankte und Angehörige sind in dieser belastenden Situation nicht allein, sondern können vielfältige Unterstützung erhalten:
- Das Pflegepersonal hilft Ihnen mit Ratschlägen und praktischen Tipps, wie Sie die Beschwerden lindern können.
- Auch das behandelnde Ärzteteam berät Sie und sagt Ihnen, welche Maßnahmen helfen können.
- Psychosoziale Krebsberatungsstellen und speziell ausgebildete Psychoonkologen können Ihnen dabei helfen, die Krankheit und ihre Folgen besser zu bewältigen.
- In der letzten Lebensphase können Sie von speziell ausgebildeten Palliative Care Teams begleitet und unterstützt werden.
Aszites ohne bekannten Ausgangstumor: CUP-Syndrom
Manche Patientinnen oder Patienten haben einen malignen Aszites, ohne dass eine Krebserkrankung bekannt ist. Die Tumoren sind dabei nicht aus Bauchfellzellen entstanden, sondern sind Metastasen. Die Besonderheit: Ärztinnen und Ärzte können den Ursprungstumor nicht finden.
Bei dieser Krankheitssituation sprechen Fachleute von einem CUP-Syndrom. CUP ist die Abkürzung für englisch "Cancer of Unknown Primary" und bedeutet "Krebs mit unbekanntem Primärtumor".
Was bedeutet das für die erkrankte Person? Ärztinnen und Ärzte versuchen, durch eine feingewebliche Untersuchung möglichst viele Eigenschaften der Krebszellen zu bestimmen. Mit vielen unterschiedlichen Untersuchungsmethoden suchen sie nach dem Ausgangstumor.
Patientinnen und Patienten brauchen viel Geduld und Ausdauer. Denn: Es kann mehrere Wochen dauern, bis alle erforderlichen Untersuchungen abgeschlossen sind.
Wichtig zu wissen
Manchmal wissen Fachleute auch nach allen Untersuchungen nicht sicher, aus welchem Organ und aus welcher Zellart die Tumoren entstanden sind. Die Untersuchungsergebnisse liefern aber Hinweise, mit denen sie die Möglichkeiten eingrenzen können.
Wie geht es weiter? Wie bei Metastasen mit bekanntem Ausgangstumor versuchen die behandelnden Ärztinnen und Ärzte, die Beschwerden zu lindern und die Tumoren wenn möglich zu entfernen. Dabei orientieren sie sich an den Informationen aus der feingeweblichen Untersuchung und verwenden Medikamente, die gegen die wahrscheinlichste Ausgangskrebsart wirksam sind.
Zum Weiterlesen
Detailwissen: Ursachen eines Aszites
Es gibt mehrere mögliche Ursachen für einen Aszites:
- Bei 7 bis 8 von 10 Erkrankten ist der Aszites eine Komplikation einer Lebererkrankung, beispielsweise einer Leberzirrhose.
- Bei 1 von 10 Erkrankten ist eine Krebserkrankung die Ursache.
- Weitere mögliche Ursachen sind beispielsweise eine Bauchfellentzündung, Komplikationen nach Operationen im Bauchraum, Unterernährung oder eine Tuberkulose des Bauchfells.
Ursachen von Aszites bei Krebserkrankten: Tumorzellen in Bauchfell und Leber
Lexikon
Peritoneum: Bauchfell, eine den Bauchraum auskleidende und die Organe umgebende Haut
Peritonealkarzinose: Befall des Bauchfells mit Tumorzellen, meist Metastasen
Bei einem malignen Aszites wachsen Krebszellen im Bauchfell (Peritonealkarzinose, Bauchfellkrebs) oder in der Leber.
Bei den meisten Erkrankten handelt es sich dabei um Absiedlungen anderer Tumoren (Metastasen). Meist liegt der Ursprungstumor im Bauchraum, zum Beispiel in den Eierstöcken, dem Gebärmutterkörper oder dem Magen-Darm-Trakt. Auch Tumoren außerhalb des Bauchraums wie zum Beispiel Brustkrebs, Lungenkrebs und Lymphome können Metastasen im Bauchfell oder der Leber bilden.
Die Tumoren können aber auch aus den Zellen des Bauchfells selber entstehen, zum Beispiel beim peritonealen Mesotheliom.
Tumoren in der Leber können auch aus den Leberzellen selbst entstehen. Dann handelt es sich um Leberzellkrebs – nicht um Lebermetastasen.
CUP-Syndrom
Ein Aszites kann auch beim CUP-Syndrom auftreten. Erkrankte haben Metastasen in Bauchfell oder Leber. Den Ursprungstumor können Ärztinnen und Ärzte jedoch nicht finden.
Mechanismus: Flüssigkeitsansammlung in der Bauchhöhle
Jeder Mensch hat Flüssigkeit im Bauchraum. Das ist normal und wichtig: Die Flüssigkeit sorgt dafür, dass die Organe im Bauchraum nicht aneinander reiben.
Bei gesunden Menschen produziert das Bauchfell eine geringe Menge Flüssigkeit. Die Lymphgefäße nehmen die gleiche Menge wieder auf und transportieren sie über das Blut ab.
Bei einem Aszites ist dieses Gleichgewicht gestört: Es gelangt mehr Flüssigkeit in die Bauchhöhle, als über die Gefäße wieder abtransportiert wird. Dadurch staut sich die Flüssigkeit im Bauchraum an.
Wie ein Aszites bei Tumorerkrankungen entsteht, ist noch nicht vollständig aufgeklärt.
Fachleute diskutieren verschiedene Mechanismen:
- Durch Metastasen in den Lymphbahnen kann die Flüssigkeit aus dem Bauchraum nicht abfließen. Auch das in der Flüssigkeit enthaltene Eiweiß kann nicht abtransportiert werden. Aufgrund des hohen Eiweißgehalts strömt noch mehr Flüssigkeit aus den Gefäßen in den Bauchraum.
- Die Tumorzellen bilden Botenstoffe, welche die Blutgefäße durchlässiger machen. Dadurch tritt mehr Flüssigkeit aus den Gefäßen in den Bauchraum aus.
- Metastasen in der Leber erhöhen den Druck in den Blutgefäßen, die Blut zur Leber führen. Dadurch gelangt mehr Flüssigkeit aus den Gefäßen in den Bauchraum.
- Metastasen beschädigen die Lymphgefäße, so dass Lymphflüssigkeit in die Bauchhöhle fließt.
Wichtig zu wissen
Fachleute gehen davon aus: Ein Aszites entsteht dann, wenn mehrere Ursachen gleichzeitig auftreten.
Quellen und Links für Interessierte und Fachkreise
Im Folgenden finden Sie eine Auswahl an hilfreichen Links zum Weiterlesen und Quellen, die für die Erstellung dieses Textes genutzt wurden.
Quellen und weiterführende Informationen
Leitlinien
Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): S3-Leitlinie Magenkarzinom, Langversion 2.0, 2019, AWMF Registernummer: 032/009OL, (abgerufen am: 27.11.2024)
Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS): S2k-Leitlinie Komplikationen der Leberzirrhose, 2019, AWMF-Nr.: 021-017 (abgerufen am: 27.11.2024)
Informationen zur Behandlung der verschiedenen Krebsarten bieten das Leitlinienprogramm Onkologie der Deutschen Krebsgesellschaft, Deutschen Krebshilfe und AWMF sowie die Leitlinien der onkopedia der Deutschen Gesellschaft für Hämatologie und Medizinische Onkologie e.V. (DGHO).
Epidemiologie
Aktuelle statistische Daten zu Krebs bietet das Zentrum für Krebsregisterdaten [LINK]. Eine Zusammenfassung bietet die Broschüre "Krebs in Deutschland für 2019/2020" [LINK] der epidemiologischen Krebsregister e. V. (GEKID) und des Zentrums für Krebsregisterdaten (ZfKD) im Robert Koch-Institut.
Fachartikel (Auswahl)
Fachdatenbank UpToDate: Runyon BA et al. (2024) Malignancy-related ascites (abgerufen am: 27.11.2024)
Geprüft
durch unsere Fachredaktion,
bestehend aus Expertinnen und Experten aus Medizin, Naturwissenschaften sowie Psychoonkologie und Recht.