- Unser Immunsystem kann prinzipiell Krebszellen erkennen und vernichten.
- Krebszellen können allerdings Ausweichstrategien gegen eine Immunantwort entwickeln.
- Wir erläutern, welche Rolle das Immunsystem bei der Krebsentstehung spielt und ob eine Immunstärkung bei der Krebsvorbeugung oder bei einer Krebserkrankung hilft.
Immunsystem und Krebs: Wichtiges in Kürze
Die bekannteste Funktion des Immunsystems ist die Abwehr von Infektionen. Weniger bekannt ist, dass das Immunsystem auch eine wichtige Rolle bei der Beseitigung von gealterten und geschädigten Zellen spielt - auch von Krebszellen. Die Zellen und Eiweiße des Immunsystems laufen im ganzen Körper "Streife" und unterscheiden "fremd" von "selbst", gesund von krank oder geschädigt. Entdecken sie Krankheitserreger oder geschädigte Zellen dann müssen sie:
- eine Infektion eindämmen und wenn möglich abwehren oder die geschädigten Zellen zerstören,
- die Immunantwort regulieren und wieder beenden, um nicht versehentlich auch gesunde körpereigene Zellen anzugreifen, und
- sich erinnern: Ein immunologisches Gedächtnis schützt vor dem erneutem Auftreten einer Krankheit.
Die Steuerung dieser Vorgänge ist komplex: Das Immunsystem soll Krankheitserreger und geschädigte Zellen angreifen und zerstören, und dies möglichst rasch. Gleichzeitig darf es aber nicht auf körpereigene gesunde Zellen mit ähnlichen Eigenschaften reagieren. Solche "falschen" Reaktionen des Immunsystems gibt es: Sie sind zum Beispiel Auslöser von Autoimmunerkrankungen wie Rheuma oder Multipler Sklerose.
An der Immunantwort sind viele verschiedene Immunzellen beteiligt. Sie alle müssen zum richtigen Zeitpunkt angeregt und dann auch wieder gehemmt werden. Die Immunantwort muss zudem in der richtigen Reihenfolge ablaufen. Daher steuern verschiedene Botenstoffe die Reaktion des Immunsystems. Interferone und Interleukine sind Beispiele für solche Botenstoffe oder "Zytokine", daneben gibt es noch weitere.
Welche Rolle spielt das Immunsystem bei Krebs?
Bei der Erkennung von Tumorzellen steht das Immunsystem vor einer schwierigen Aufgabe: Krebszellen sind körpereigene Zellen. Der eigene Körper soll jedoch normalerweise nicht angegriffen werden.
Im Vergleich zu gesunden Zellen tragen Tumorzellen allerdings mehr oder weniger große Veränderungen. Daher ist das Immunsystem eigentlich dazu in der Lage, solche "kranken" Zellen zu erkennen und zu vernichten. Das passiert bei gesunden Menschen auch regelmäßig - ohne dass man etwas davon merkt.
Das Problem: Krebszellen können Ausweichstrategien gegen eine Immunantwort entwickeln. Zum Beispiel indem sie sich "unsichtbar" für das Immunsystem machen. Oder indem sie die Immunreaktion hemmen. So können sie der Immunabwehr entkommen.
Wichtig für Betroffene ist: Ihr Immunsystem hat nicht pauschal "versagt", wenn Krebs entsteht. Es ist auch nicht unbedingt zu geschwächt, um den Tumor bekämpfen zu können.
- Deshalb ist es in den allermeisten Fällen auch weder notwendig noch möglich, das Immunsystem ungezielt zu stimulieren, um Krebs zu bekämpfen.
Mediziner gehen davon aus: Eine ungezielte "Immunstärkung" könnte unter Umständen sogar gefährlich sein - beispielsweise für Patienten mit bestimmten Lymphomformen, bei denen die Immunzellen selbst Träger der Krebserkrankung sind.
Kann man mit Immuntherapien Krebs bekämpfen?
Seit langem versuchen Wissenschaftler, die fehlende Immunreaktion auf Krebszellen künstlich zu erzeugen. Die Hoffnung: mit gezielten immunologischen Therapien das Tumorwachstum zu bremsen oder sogar ganz aufhalten zu können. Einige Ansätze haben in der Vergangenheit nicht den erhofften Erfolg gezeigt. Je mehr über die körpereigenen Abwehrmechanismen bekannt ist, desto besser kann man jedoch neue Strategien entwickeln: Mit ihnen kann man gezielter in die Mechanismen der Immunabwehr gegen Krebs eingreifen.
Für diese neuen Ansätze gilt:
- Bisher gibt es noch nicht sehr viele zugelassene Medikamente. Sie sind nur bei wenigen Tumorarten für Betroffene mit fortgeschrittener Erkrankung geeignet. Sie wirken auch nur bei einem Teil der Patienten - zeigt sich allerdings eine Wirkung, dann kann diese lange anhalten.
- Ansätze zur "therapeutischen Impfung gegen Krebs" bei einer bereits bestehenden Krebserkrankung müssen dagegen überwiegend noch weiter erforscht werden und sind bisher kein Standard in der Krebstherapie.
- Weitere Therapieansätze werden noch in der Grundlagenforschung oder in klinischen Studien geprüft.
Aus der Forschung haben sich auch Erkenntnisse ergeben, die Krebspatienten auf andere Weise zugutekommen. Ein Beispiel: Viele neue zielgerichtete Medikamente sind Antikörper - also Eiweiße, die natürlicherweise von Immunzellen gebildet werden. Die künstlich hergestellten Antikörper richten sich gegen veränderte Strukturen in oder an den Krebszellen. Das bedeutet: Statt das körpereigene Immunsystem eines Patienten oder einer Patientin zu aktivieren, gibt man gezielt hergestellte Antikörper gleich als Medikament.
So funktioniert das Immunsystem
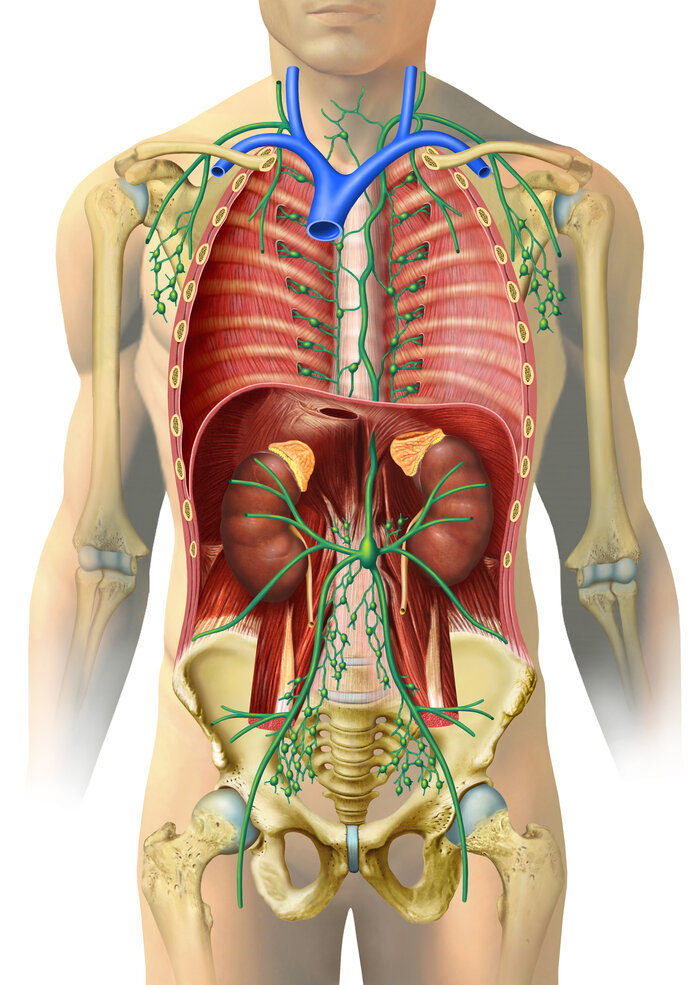
Bild: © Frank Geisler
Das Immunsystem ist ein Netzwerk aus verschiedenen Organen, Zellen und Eiweißmolekülen, das im ganzen Körper Krankheitserreger, Fremdstoffe und defekte Zellen aufspürt und entfernt.
Die meisten Bakterien vermehren sich überwiegend in den Körperflüssigkeiten, etwa im Blut oder in Gewebsflüssigkeit. Viren ziehen sich dagegen zur Vermehrung ins Innere von Körperzellen zurück. Aus diesem Grund hat das Immunsystem zwei verschiedene Abwehrstrategien parat:
- Humorale Abwehr: Als humorale Immunantwort wird der Teil der Immunabwehr bezeichnet, der nicht direkt durch Immunzellen vermittelt wird. Sie wirkt vor allem gegen Krankheitserreger in Körperflüssigkeiten. "Humor" ist lateinisch und bedeutet "Körperflüssigkeit".
Bestandteile der humoralen Abwehr sind zum Beispiel die Antikörper, große und sehr spezifische Eiweißmoleküle, mehr dazu in einem eigenen Abschnitt.
Wichtig ist auch das sogenannte Komplementsystem: Dabei handelt es ebenfalls um im Blut und im ganzen Körper verbreitete Eiweißverbindungen. Sie binden an Krankheitserreger und andere Fremdstoffe. Allein schon durch die Anbindung können sie diese unschädlich machen. Sie markieren die Fremdstoffe durch die Kopplung aber auch für die Zellen des Immunsystems. - Zelluläre Abwehr: Die dazugehörigen Zellen sind für die Beseitigung infizierter Gewebe und kranker, gealterter oder anderweitig geschädigter Zellen zuständig. Sie dienen also auch der Entfernung von Krebszellen. Mehr zur zellulären Abwehr und den dazu gehörigen verschiedenen Immunzellen bietet ein eigener Abschnitt.
Organe und Gewebe des Immunsystems: Die Immunzellen selbst entwickeln sich in spezialisierten Organen und Geweben. Dazu gehören das Knochenmark und der Thymus, auch Bries genannt.
- Im Knochenmark entstehen die sogenannten Stammzellen des blutbildenden Systems. Außerdem entstehen und reifen hier spezialisierte weiße Blutkörperchen, die B-Zellen. Das "B" steht für "bone marrow", englisch für Knochenmark.
- Im Thymus entwickeln sich die verschiedenen T-Zellen. Das "T" steht für Thymus.
Von ihrem Entstehungsort aus gelangen die Immunzellen über das Blut und die Lymphbahnen in alle Organe und Gewebe des Körpers.
Weitere Organe und Gewebe des Immunsystems sind die Milz, alle Lymphknoten und Lymphbahnen und die Rachen- und Gaumenmandeln (Tonsillen). Hinzu kommt lymphatisches Gewebe in weiteren Schleimhäuten, vor allem im Darm. Diese Gewebe dienen unter anderem als Filterstationen für Eindringlinge in den Körper. Dort konzentrieren sich Zellen des Immunsystems. Einige Zelltypen durchlaufen hier auch letzte Reifungsschritte.
So entstehen Immunzellen

Bild: © Krebsinformationsdienst, DKFZ
Alle Zellen des Immunsystems entstehen aus sogenannten Stammzellen im Knochenmark. Aus diesen Stammzellen können aber auch alle anderen Blutzelltypen wie rote Blutkörperchen und Blutplättchen entstehen. Fachleute bezeichnen diese Alleskönner daher als "pluripotent".
Die Entwicklung verläuft in mehreren Schritten: Aus den Stammzellen entwickeln sich zunächst die direkten Vorläuferzellen der roten Blutkörperchen, der Blutplättchen und der beiden Hauptgruppen der weißen Blutkörperchen.
- Rote Blutkörperchen (Erythrozyten) sind für den Sauerstofftransport im Blut verantwortlich. Ist ihre Zahl zu gering, leidet man unter Umständen unter Sauerstoffmangel und fühlt sich müde.
- Blutplättchen (Thrombozyten) sind für die Blutgerinnung zuständig. Fehlen sie, kann selbst eine harmlose Verletzung zu unstillbaren Blutungen führen.
- Weiße Blutkörperchen (Leukozyten) sind Teil des Immunsystems. Es gibt verschiedene Zelltypen mit unterschiedlichen Aufgaben bei der Abwehr von Infektionen und der Beseitigung von geschädigten Zellen.
Leukozyten: Welche Zellen sind im Einzelnen an der Immunantwort beteiligt?
B-Lymphozyten oder B-Zellen sind zuständig für die Bildung von Antikörpern gegen fremde Strukturen im Körper, beispielsweise gegen Krankheitskeime. Aktive B-Zellen, die großen Mengen an Antikörpern bilden, nennt man auch Plasmazellen. Langlebige B-Gedächtniszellen bleiben nach einer überstandenen Infektion im Körper. Sie können bei erneutem Kontakt mit einem ihnen bekannten Fremdkörper innerhalb weniger Stunden eine Immunreaktion auslösen, die das Ausbrechen einer Infektion verhindert.
T-Lymphozyten oder T-Zellen werden noch weiter unterteilt. Eine wichtige Funktion haben die zytotoxischen T-Zellen. Sie erkennen und zerstören vor allem von Viren befallene sowie geschädigte Körperzellen. Sie können daher auch Tumorzellen zerstören. T-Helferzellen bilden Botenstoffe, die andere Immunzellen aktivieren - beispielsweise Makrophagen und B-Zellen. Regulatorische T-Zellen hemmen die T-Zell-Reaktion. Sie sorgen dafür, dass das Immunsystem nicht auf den eigenen Körper losgeht. Bei Krebs ist diese Schutzfunktion jedoch ein Problem: Unter Umständen verhindern regulatorische T-Zellen auch eine Immunantwort auf Tumorzellen. T-Gedächtniszellen bilden ebenfalls ein "immunologisches Gedächtnis".
Natürliche Killerzellen (NK-Zellen) greifen virusinfizierte Zellen an. Sie können auch Tumorzellen bekämpfen.
Monozyten sind die Vorläuferzellen der Makrophagen. Diese Fresszellen erkennen und "fressen" ins Gewebe eingedrungene Erreger und aktivieren weitere Immunzellen.
Dendritische Zellen sind darauf spezialisiert, Fremdstoffe aufzunehmen und den Lymphozyten zur Erkennung zu präsentieren. Diese Fremdstoffe nennt man auch "Antigene". Zum Antigen kann sehr vieles werden: Fremdeiweiße auf der Oberfläche von Blütenpollen, Virusproteine, aber auch Strukturen auf menschlichen Zellen.
Granulozyten: Dazu gehören die neutrophilen, die basophilen sowie die eosinophilen Zellen. Sie sind unter anderem auf die Erkennung und Abwehr von Bakterien oder Parasiten spezialisiert. Sie können aber auch zu einer allergischen Reaktion beitragen.
Mastzellen erkennen Parasiten und Fremdstoffe und setzen daraufhin Botenstoffe frei. Sie spielen eine wichtige Rolle bei allergischen Reaktionen.
Zelluläre Abwehr: So erkennt der Körper infizierte oder defekte Zellen
Defekte Zellen erkennen
Woran erkennt der Körper virusinfizierte oder geschädigte Zellen? Sie machen selbst auf sich aufmerksam: Sie präsentieren auf ihrer Zellhülle typische Eiweiße, wie eine Art "Fahne". Diese Signale können eine Immunreaktion auslösen.
Viren und auch manche Bakterien halten sich im Inneren der von ihnen befallenen Zellen auf. Für das Immunsystem sind sie damit zunächst unsichtbar. Und: Um die Eindringlinge zu erreichen und loszuwerden, ist es notwendig, die gesamte infizierte Zelle zu zerstören. Auch Tumorzellen müssen vollständig beseitigt werden.
Wie erkennen die Immunzellen, ob eine Zelle geschädigt ist und zerstört werden muss? Jede Zelle hat normalerweise auf ihrer Oberfläche sehr typische Eiweißmoleküle, wie eine Art Fahne. Träger dieser "Fahne" ist der Haupthistokompatibilitätskomplex (MHC, vom Englischen Major Histocompatibility Complex). Die präsentierten Eiweißstücke stellen ein Abbild oder eine Art Muster der in der Zelle hergestellten Eiweiße dar.
- Funktioniert eine Zelle so, wie sie soll, lässt sich dies an der MHC-"Fahne" ablesen.
- Ist eine Zelle von einem Virus befallen oder anderweitig abnormal, werden mithilfe der MHC-Moleküle auch die fremden Eiweiße vorgezeigt. Diese lösen eine Immunreaktion aus, durch die letztendlich die gesamte Zelle abgebaut wird.
Antikörper: Passgenaue Abwehr gegen Fremdstoffe
Lexikon
Antigen: Merkmal, das vom Immunsystem erkannt wird: beispielsweise Teile von Krankheitserregern oder Fremdstoffen
Antikörper: körpereigene Eiweiße, die Antigene erkennen und spezifisch binden
Antikörper sind Y-förmige Eiweißmoleküle. Man nennt diese Proteine auch Immunglobuline. Sie haben eine wichtige Funktion bei der Abwehr von Krankheitserregern: Sie erkennen körperfremde und gegebenenfalls auch veränderte körpereigene Strukturen, sogenannte Antigene. Heftet sich ein Antikörper an einem Antigen fest, ist das ein Start-Signal für weitere Immunreaktionen.
Wie schafft es der Körper, innerhalb kürzester Zeit eine hochspezifische Immunantwort zu leisten? Er nutzt eine Art Baukasten, um die Immunreaktion schnell und gezielt anpassen zu können. Ein Antikörper besteht deshalb aus mehreren Abschnitten, die zusammen ein "Y" bilden (siehe Bild):
Die "variable Region", auch "V"-Region genannt, unterscheidet sich von Antikörper zu Antikörper, sie passt immer nur zu einem ganz bestimmten Fremdstoff. Dort wird das fremde Antigen spezifisch gebunden.
Die "konstante Region", das Bein des Antikörper-"Y", ist bei Weitem nicht so variabel: Es gibt nur wenige Versionen. Der Körper nutzt sie als Baustein für unterschiedliche Antikörper. Sie wird zum Beispiel von Immunzellen erkannt und gebunden.
Antikörper werden von B-Zellen gebildet
Jede B-Zelle produziert nur einen Typ Antikörper, der in der Regel nur ein ganz bestimmtes fremdes Merkmal erkennt. Beispielsweise können Antikörper gegen Keuchhustenbakterien keine Salmonellen erkennen.
Hat eine B-Zelle mit der Antikörperproduktion begonnen und teilt sich weiter, produzieren auch ihre aus der Zellteilung hervorgegangenen Nachkommen denselben Antikörper: Fachleute sprechen von einem "B-Zell-Klon".
Hatte der Körper schon einmal Kontakt mit einer fremden Struktur? War die Antikörperproduktion schon einmal angelaufen? Dann stellen spezialisierte B-Zellen eine Art Gedächtnis für dieses Antigen dar: Kommt der Körper erneut mit dem Eindringling in Kontakt, können diese langlebigen B-Zellen sehr schnell wieder mit der Antikörperproduktion beginnen. Diesen Effekt nutzt man zum Beispiel bei Impfungen gegen Infektionskrankheiten aus.
Immunabwehr: angeborener und erworbener Schutz
Das Immunsystem ist anpassungsfähig
Überstandene Infektionen und Schutzimpfungen trainieren die Abwehr des Körpers.
Ein Teil des Schutzes vor Krankheitserregern und anderen schädlichen Einflüssen ist angeboren und verändert sich im Laufe des Lebens wenig: Haut und Schleimhäute bilden wirksame Barrieren. In Speichel und Magensäure befinden sich Enzyme, Säuren und andere Stoffe, die Krankheitserreger bekämpfen.
Auch ein Teil der eigentlichen Immunabwehr muss nicht extra trainiert werden, sondern ist angeboren: Das Komplementsystem reagiert relativ unspezifisch auf Mikroorganismen. Fresszellen und natürlichen Killerzellen reicht das Signal "fremd", um aktiv zu werden. Ihre schnelle Reaktion - innerhalb von Minuten bis Stunden - soll Viren und Bakterien schon beim ersten Eindringen in den Körper abwehren und an der Vermehrung hindern.
Die Merkmale, auf die diese angeborene Immunantwort reagiert, sind nicht sehr spezifisch, aber sehr typisch für viele Krankheitserreger. Diese Teile der Immunabwehr sind daher ständig und sofort einsatzbereit.
Anders sieht es aus, wenn der Körper erstmals mit etwas in Kontakt kommt, dem diese typischen Merkmale fehlen. Dann muss der Körper eine Immunantwort "maßschneidern", etwa durch die erstmalige Produktion passender Antikörper. Die dabei aktiven Mechanismen nennt man erworbene oder adaptive Immunantwort. Wichtige Träger dieser Reaktion sind die B- und T-Lymphozyten. Sie bilden später auch das immunologische Gedächtnis, das bei erneutem Kontakt schnell reagieren kann.
Das bedeutet: Das Immunsystem entwickelt sich im Laufe des Lebens immer weiter.
- Als Training dient jede überstandene Infektion, jeder Kontakt mit körperfremden Stoffen und Krankheitserregern, aber auch jede Schutzimpfung.
Kann man sein Immunsystem selbst beeinflussen? Das Immunsystem ist auch abhängig vom Allgemeinzustand, insbesondere von einer ausgewogenen Ernährung. Ist jemand beispielsweise stark unterernährt, stehen dem Körper nicht genug Ressourcen für eine ausreichende Immunantwort zur Verfügung, also zum Beispiel Proteine für die Produktion vieler Immunzellen und Antikörper. Studien zeigen, dass auch ausreichend Bewegung und Schlaf das Immunsystem positiv beeinflussen können. Die zugrunde liegenden Mechanismen versteht man noch nicht in allen Details, ähnlich wie den Zusammenhang mit dem psychischen Befinden.
Kein hundertprozentiger Schutz
Auch sehr gesunde Kinder und Erwachsene müssen mit gelegentlichen Infektionserkrankungen rechnen, etwa einem Schnupfen. Fachleuten zufolge gelten etwa zwei bis vier harmlosere Infektionen im Jahr für Erwachsene als normal. Bei Kleinkindern und Säuglingen gehen Kinderärzte sogar von acht bis zwölf Atemwegs- oder Magen-Darm-Infekten aus, ohne Alarm zu schlagen: Die Immunabwehr funktioniert bei den meisten Menschen trotzdem gut und bedarf keiner besonderen Unterstützung.
Immunschwäche und Risiko für Krebs
Ist ein schwaches Immunsystem ein Krebsrisiko? Dabei muss man zunächst unterscheiden, ob die Immunabwehr nur vorübergehend nicht ausreichend arbeitet oder ob das Problem lebenslang besteht.
Dauerhafte oder zumindest länger anhaltende Immunstörungen sind eher selten. Dazu zählen zum Beispiel seltene angeborene Immundefekte, bei denen man die genetischen Ursachen heute relativ gut kennt. Betroffene Menschen sind meist schon in der Kindheit sehr anfällig für Infekte, die noch dazu meist schwerer verlaufen als normalerweise. Für manche dieser Erkrankungen ist bekannt, dass auch das Krebsrisiko Betroffener steigt.
Unter den schweren erworbenen, also nicht angeborenen Immunschwächeerkrankungen ist eine Infektion mit HI-Viren und in der Folge eine AIDS-Erkrankung die weltweit häufigste: HI-Viren befallen die Zellen des Immunsystems und legen so das Immunsystem lahm. Die Abkürzung HIV steht entsprechend für "Humane Immundefizienz-Viren". Von Patienten mit einer unbehandelten HIV-Infektion weiß man anhand der vorliegenden Statistiken zurzeit am besten, dass bei ihnen auch das Krebsrisiko steigt. Dabei spielen anscheinend vor allem Viren eine Rolle, die das Risiko für einige Tumorarten steigern, mehr dazu im Text "HIV und AIDS: Steigert die Infektion das Krebsrisiko?".
Ähnliche Studien gibt es für Patienten nach einer Organtransplantation. Um eine Abstoßung des Spenderorgans zu vermeiden, müssen sehr viele Betroffene lebenslang Medikamente zur Unterdrückung des Immunsystems einnehmen. Auch ihr Krebsrisiko steigt - und auch hier sind es vor allem Krebsarten, die mit einer Virusinfektion als Auslöser in Verbindung gebracht werden.
Vorübergehende Probleme mit der Abwehr sind insgesamt zwar häufiger. Allerdings sind ihre Auswirkungen auf das langfristige Krebsrisiko statistisch nur schlecht fassbar.
- Ernsthafte Probleme mit der Immunabwehr haben zum Beispiel Menschen, denen es körperlich sehr schlecht geht oder die stark mangelernährt sind.
- Eine weitere Ursache sind einige Medikamente und andere Therapien, die die Immunfunktion beeinträchtigen können. Ein Beispiel aus der Krebsmedizin sind höher dosierte Chemotherapien oder sehr umfangreiche Bestrahlungen. Für Betroffene ist wichtig: Der Körper erholt sich von dieser vorübergehenden Immunschwäche, meist auch ohne besondere Maßnahmen.
- Auch Leukämie- und Lymphomerkrankungen beeinträchtigen die Immunabwehr, denn die Immunzellen selbst sind die Träger der bösartigen Veränderungen. Ihre Funktion ist gestört, und die Krebszellen verdrängen noch dazu gesunde Immunzellen. Die Therapie zielt darauf ab, die Blutbildung und damit auch die Immunfunktion wieder zu normalisieren.
Immunsystem und Krebs: Wenn Krebszellen unentdeckt bleiben
Das Immunsystem kann veränderte Zellen wie Krebszellen in den allermeisten Fällen erkennen und vernichten. Dieser Prozess ist vermutlich sogar der Normalfall, ohne dass man etwas davon spürt - sonst wäre Krebs noch sehr viel häufiger.
Doch was ist passiert, wenn Krebszellen der Immunabwehr entkommen? Tumorzellen sind für das Immunsystem nicht so fremd wie Bakterien, Viren oder Pilze: Sie tragen im Vergleich zu diesen Eindringlingen immer noch sehr viele Merkmale des Gewebes, aus dem sie ursprünglich stammen. Das macht es für die Abwehr schwieriger, sie zu erkennen. Hinzu kommt: Krebszellen verändern sich sehr schnell und können dadurch Merkmale, die sie als defekt kennzeichnen, auch verlieren oder verstecken.
Wie entgehen Krebszellen dem Immunsystem?
Krebszellen können sich tarnen
Fehlen den Tumorzellen auffällige Signale, behandelt das Immunsystem die Zellen wie gesundes Gewebe.
Entkommen Krebszellen dem Immunsystem, ist das nicht auf eine gezielte Strategie zurückzuführen. Vielmehr führt eine Reihe zufälliger Veränderungen dazu, dass das Immunsystem die Tumorzellen nicht mehr als geschädigt erkennt - oder sie trotz Erkennung nicht angreift. Krebs ist also bei den allermeisten Patienten keine Folge eines Immundefekts oder einer pauschalen Immunschwäche.
Hier einige Beispiele für solche Veränderungen:
- Die Tumorzellen tarnen sich: Manche Krebszellen zeigen keine tumortypischen Erkennungsmerkmale mehr vor. Andere tragen Merkmale, die eigentlich für gesunde Gewebe typisch sind.
- Tumorzellen können das Immunsystem direkt manipulieren oder schwächen. Zwar erkennt das Immunsystem die Tumorzellen noch. Es kann sie jedoch nicht mehr angreifen.
Hier einige Beispiele: Tumorzellen können auf ihrer Oberfläche Merkmale tragen, die die Aktivität von T-Lymphozyten abschwächen. Oder sie bilden Botenstoffe, die die Reifung oder die Aktivität von Immunzellen hemmen. Oder sie mobilisieren regulatorische T-Zellen: Diese Zellen sind normalerweise dafür zuständig, unerwünschte Immunreaktionen zu unterdrücken und eigenes Gewebe zu schützen. Durch die Aktivierung wird auch die Immunantwort gegen geschädigte und veränderte Zellen wie Krebszellen unterdrückt. - Tumorzellen können auch andere Zellen in ihrer Umgebung dazu nutzen, das Immunsystem zu schwächen: Beispielsweise regen manche Tumoren in ihrer Umgebung die Vermehrung von unreifen Knochenmarkszellen an, den sogenannten myeloiden Suppressorzellen. Diese Zellen können die Aktivität von T-Zellen herabsetzen.
Chronische Entzündungen: Mögliche Rolle des Immunsystems bei der Krebsentstehung
Kann das Immunsystem auch Krebs fördern? Schon vor mehr als 150 Jahren vermutete der Arzt Rudolf Virchow einen Zusammenhang zwischen Entzündungen und Krebs. Inzwischen gibt es deutliche Hinweise darauf, dass zumindest chronische - also lang anhaltende oder dauerhafte - Entzündungen zur Entstehung von Krebs beitragen können. Beispielsweise haben Betroffene mit der chronisch entzündlichen Darmerkrankung Colitis ulcerosa ein erhöhtes Risiko für Darmkrebs. Das Risiko scheint vor allem von der Dauer des Reizzustandes abzuhängen. Man weiß allerdings auch: Nicht jede dauerhafte Entzündung führt zu Krebs.
Was ist der Grund dafür, dass Krebs aufgrund einer chronischen Entzündung entstehen kann? Eine Entzündungsreaktion wird von Zellen des Immunsystems hervorgerufen: Ist Gewebe gereizt, wandern sie in die betroffene Region ein. Bei einer chronischen Entzündung sind dauerhaft Immunzellen aktiviert und schütten verschiedene Botenstoffe und andere Substanzen aus. Wie diese zur Krebsentstehung beitragen, ist noch nicht restlos verstanden.
Zum Beispiel vermuten Wissenschaftler: Immunzellen schütten während einer Entzündungsreaktion auch Substanzen aus, die das Erbmaterial von Zellen schädigen können. Sterben die geschädigten Zellen in der Folge nicht ab, können sie sich zu Krebszellen entwickeln. Eingewanderte Immunzellen bilden noch weitere Stoffe, die auf unterschiedliche Weise zur Entstehung und Weiterentwicklung von Krebs beitragen können - zum Beispiel solche, die das Selbstmordprogramm von Tumorzellen hemmen oder sie zur Zellteilung anregen. Weitere Forschung ist aber notwendig, um besser zu verstehen, wie dauerhafte Entzündungen Krebs fördern.
Zum Weiterlesen
Immuntherapie: mit dem Immunsystem den Krebs bekämpfen
Immunologische Ansätze in der Krebstherapie
Es gab bereits viele verschiedene Ideen, wie man das Immunsystem auf einen Tumor ansetzen könnte. Nicht alle konnten jedoch erfolgreich angewendet werden. Neuere Ansätze sind vielversprechend. Allerdings kommt bisher nur für wenige Patienten eine gezielte Immuntherapie infrage.
Seit mehr als hundert Jahren versucht man, Krebs mit immunologischen Methoden zu behandeln – zum Teil mit Erfolg, zum Teil aber auch nicht: Längst nicht alle erforschten Methoden lassen sich vom Labor in die Praxis übertragen.
Versuche zeigen, dass man sehr wohl Immunreaktionen auf Tumoren auslösen kann. Ältere Ansätze erwiesen sich allerdings häufig als nicht stark genug, um als alleinige Therapie zu wirken. Daher versucht man heute zum Beispiel, Methoden wie Bestrahlung oder Chemotherapie mit Immuntherapien oder verschiedene Immuntherapie-Methoden miteinander zu kombinieren. Außerdem wurden neuere Ansätze entwickelt, die spezifischer in die Immunantwort gegen den Tumor eingreifen - mit teilweise guten Ergebnissen.
Immunologische Behandlungen haben zurzeit allerdings nicht bei allen Tumorarten einen Stellenwert. Auch bei Krebsformen, bei denen es entsprechende Therapieansätze gibt, kommen diese nicht für jeden betroffenen Patienten oder in jedem Krankheitsstadium infrage.
Zu den immunologischen Strategien, die Wissenschaftler und Ärzte erforschen und einsetzen, gehören:
- Zytokine zur Immunstimulation: Diese Botenstoffe des Immunsystems werden schon seit Längerem zur Krebstherapie eingesetzt. Sie haben allerdings die anfangs in sie gesetzten großen Hoffnungen nicht erfüllt: Zytokine wie Interferone und Interleukine wirken nur bei wenigen Tumorarten und auch da nicht bei allen Patienten. Sie werden zunehmend durch neuere, besser wirksame Medikamente ersetzt.
- Erkennen von Tumorantigenen: Verschiedene Strategien setzen auf die bessere Erkennung von Merkmalen, die typisch für Krebszellen sind. Fachleute sprechen von "tumorspezifischen" oder "tumorassoziierten" Antigenen (TSA beziehungsweise TAA). Sie kommen entweder gar nicht auf gesunden Körperzellen vor oder in anderer Form oder Häufigkeit. Zum Beispiel können in Krebszellen Programme aus der Embryonalentwicklung wieder angeworfen werden, die in "erwachsenen" Zellen völlig fehl am Platz sind. Oder ein Merkmal wird durch die Vervielfachung seines Bauplans in der Erbsubstanz viel zu oft produziert.
In der Krebsmedizin spielen Tumorantigene eine weitere wichtige Rolle: Manche von ihnen eignen sich als Tumormarker in der Diagnostik und Verlaufskontrolle. - "Krebs-Impfung": Um das Immunsystem auf Tumorantigene "anzusetzen", testen Wissenschaftler und Ärzte verschiedene Strategien. Zum Beispiel kann man diese für den Tumor charakteristischen Erkennungszeichen oder ihren Bauplan impfen. Die Hoffnung: Erhält der Patient die typischen Tumorantigene in hoher Dosierung und zusammen mit Wirkungsverstärkern, fällt es dem Immunsystem leichter, darauf zu reagieren. In weiteren Ansätzen werden Patienten eigene Immunzellen entnommen, verändert oder mit Antigenen beladen, vervielfältigt und dann den Betroffenen zurückgegeben.
Solche Ansätze gehören bisher überwiegend nicht zu den Standardmethoden in der Krebstherapie, mehr dazu im Text "Immuntherapien".
Im weiteren Sinn könnte man auch eine Impfung zum Schutz vor einer Infektion mit krebsfördernden Viren als "Krebs-Impfung" bezeichnen, mehr dazu im Text "Viren als Krebsrisiko". - Antikörper: Statt das körpereigene Immunsystem auf Tumorantigene anzusetzen, können Betroffene auch "vorproduzierte" Antikörper gegen typische Merkmale als Medikament erhalten. Diese lösen mit ihrer Bindung an die Tumorzellen unter anderem auch eine gewisse Immunreaktion aus. Die Hauptwirkung vieler solcher Antikörper besteht aber darin, dass sie gezielt in Abläufe eingreifen, die für Wachstum oder Stoffwechsel von Tumorzellen wichtig sind. Solche Behandlungsverfahren zählen daher zu den sogenannten zielgerichteten Therapien, die einen wachsenden Stellenwert in der Krebsbehandlung haben. Mehr zum Thema finden Interessierte im Text "Zielgerichtete Krebsmedikamente: Targeted Therapies".
Immun-Checkpoint-Inhibitoren: Es gibt allerdings auch Antikörper, die extra dafür entwickelt wurden, das Immunsystem zu aktivieren: Diese Antikörper bezeichnen Fachleute als "Immun-Checkpoint-Inhibitoren". Sie richten sich gegen körpereigene "Bremsen" im Immunsystem und verhindern so eine Unterdrückung der Immunantwort durch die Tumorzellen, mehr dazu im Text "Immuntherapien". Bisher sind erst wenige solcher Checkpoint-Hemmer zur Krebstherapie zugelassen, weitere werde aber intensiv in Studien geprüft.
Bispezifische Antikörper: Auch diese zählen zu den Immuntherapien: Sie haben auf ihren beiden Armen verschiedene Bindungsstellen, eine für ein Tumorantigen und eine für Immunzellen. Damit sollen sie Immunzellen zu den Tumorzellen locken, die diese dann zerstören. - Stammzelltransplantation: Im weitesten Sinn zählt auch die Transplantation von Knochenmark- oder Blutstammzellen zu den Immuntherapien: Sie wird eingesetzt, wenn bei Patienten mit bestimmten Leukämien oder Lymphomen das erkrankte Knochenmark durch eine Hochdosischemo- oder Strahlentherapie zerstört werden muss. Um die Produktion von neuen Blut- und Immunzellen zu ermöglichen, erhalten Patienten danach Knochenmark oder Stammzellen von einem Spender. Heute weiß man: Die von einem fremden Spender transplantierten Immunzellen greifen auch verbliebene Krebszellen des Empfängers an. Allerdings kann sich das "neue" Immunsystem auch gegen gesundes Gewebe des Empfängers richten: Solche Immunreaktionen gehören zu den kritischen Nebenwirkungen einer Stammzelltransplantation.
Quellen und Links für Interessierte und Fachkreise
Im Folgenden finden Sie eine Auswahl an hilfreichen Links zum Weiterlesen und Quellen, die für die Erstellung dieses Textes genutzt wurden.
Leitlinien, Fachgesellschaften
Behandlungsleitlinien deutscher Fachgesellschaften sind unter anderem abrufbar auf den Internetseiten der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V. (www.awmf.org/leitlinien.html), darunter auch Leitlinien zu Immundefekten.
Weiterführende Informationen zum Thema bieten auch die Deutsche Gesellschaft für Immunologie (www.dgfi.org/index.php) oder zum Beispiel die Internationale Union Immunologischer Gesellschaften (International Union of Immunological Societies IUIS, www.iuisonline.org).
Überblicksliteratur und Fachbücher zum Thema
Fachveröffentlichungen sind über wissenschaftliche Bibliotheken oder kostenpflichtige Onlinedienste zugänglich, bei einigen sind auch Abstracts oder Volltexte frei verfügbar. Als Hilfestellung hat der Krebsinformationsdienst praktische Tipps in einem Informationsblatt zum Laden oder Ausdrucken zusammengefasst: "Medizinische Fachliteratur: Artikel in Literaturdatenbanken suchen" (PDF).
Balkwill FR, Capasso M, Hagemann T. The tumor microenvironment at a glance. Journal of Cell Science 2012; 125: 5591–5596. doi: 10.1242/jcs.116392.
Beatty GL, Gladney WL. Immune escape mechanisms as a guide for cancer immunotherapy. Clin Cancer Res. 2015 Feb 15;21(4):687-92. doi: 10.1158/1078-0432.CCR-14-1860.
Bhatia A, Kumar Y. Cellular and molecular mechanisms in cancer immune escape: a comprehensive review. Expert Rev Clin Immunol. 2014 Jan;10(1):41-62. doi: 10.1586/1744666X.2014.865519.
Dubrow R, Silverberg MJ, Park LS, Crothers K, Justice AC. HIV infection, aging, and immune function: implications for cancer risk and prevention. Curr Opin Oncol. 2012 Sep;24(5):506-16. doi: 10.1097/CCO.0b013e328355e131
Candeias SM, Gaipl US. The Immune System in Cancer Prevention, Development and Therapy. Anticancer Agents Med Chem. 2016;16(1):101-7. doi: 10.2174/1871520615666150824153523
Cavallo F, De Giovanni C, Nanni P, Forni G, Lollini PL. 2011: the immune hallmarks of cancer. Cancer Immunol Immunother. 2011 Mar;60(3):319-26. doi: 10.1007/s00262-010-0968-0.
Chai EZ, Siveen KS, Shanmugam MK, Arfuso F, Sethi G. Analysis of the intricate relationship between chronic inflammation and cancer. Biochem J. 2015 May 15;468(1):1-15. doi: 10.1042/BJ20141337.
Corthay A. Does the immune system naturally protect against cancer? Front Immunol. 2014 May 12;5:197. doi: 10.3389/fimmu.2014.00197.
Cutrell J, Bedimo R. Non-AIDS-defining cancers among HIV-infected patients. Curr HIV/AIDS Rep. 2013 Sep;10(3):207-16. doi: 10.1007/s11904-013-0166-8.
Grivennikov SI, Greten FR, Karin M. Immunity, inflammation, and cancer. Cell. 2010 Mar 19;140(6):883-99. doi: 10.1016/j.cell.2010.01.025.
Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell. 2011 Mar 4;144(5):646-74. doi: 10.1016/j.cell.2011.02.013.
Lakshmi Narendra B, Eshvendar Reddy K, Shantikumar S, Ramakrishna S. Immune system: a double-edged sword in cancer. Inflamm Res. 2013 Sep;62(9):823-34. doi: 10.1007/s00011-013-0645-9.
Mittal D, Gubin MM, Schreiber RD, Smyth MJ. New insights into cancer immunoediting and its three component phases--elimination, equilibrium and escape. Curr Opin Immunol. 2014 Apr;27:16-25. doi: 10.1016/j.coi.2014.01.004.
Ribas A. Adaptive Immune Resistance: How Cancer Protects from Immune Attack. Cancer Discov. 2015 Sep;5(9):915-9. doi: 10.1158/2159-8290.CD-15-0563.
Schreiber RD, Old LJ, Smyth MJ. Cancer immunoediting: integrating immunity's roles in cancer suppression and promotion. Science. 2011 Mar 25;331(6024):1565-70. doi: 10.1126/science.1203486.
Shalapour S, Karin M. Immunity, inflammation, and cancer: an eternal fight between good and evil. J Clin Invest. 2015 Sep;125(9):3347-55. doi: 10.1172/JCI80007.
Stockmann C, Schadendorf D, Klose R, Helfrich I. The impact of the immune system on tumor: angiogenesis and vascular remodeling. Front Oncol. 2014 Apr 8;4:69. doi: 10.3389/fonc.2014.00069.
Sukari A, Nagasaka M, Al-Hadidi A, Lum LG. Cancer Immunology and Immunotherapy. Anticancer Res. 2016 Nov;36(11):5593-5606.
Vinay DS, Ryan EP, Pawelec G, Talib WH, Stagg J, Elkord E, Lichtor T, Decker WK, Whelan RL, Kumara HM, Signori E, Honoki K, Georgakilas AG, Amin A, Helferich WG, Boosani CS, Guha G, Ciriolo MR, Chen S, Mohammed SI, Azmi AS, Keith WN, Bilsland A, Bhakta D, Halicka D, Fujii H, Aquilano K, Ashraf SS, Nowsheen S, Yang X, Choi BK, Kwon BS. Immune evasion in cancer: Mechanistic basis and therapeutic strategies. Semin Cancer Biol. 2015 Dec;35 Suppl:S185-98. doi: 10.1016/j.semcancer.2015.03.004. Epub 2015 Mar 25.
Woo SR, Corrales L, Gajewski TF. Innate immune recognition of cancer. Annu Rev Immunol. 2015;33:445-74. doi: 10.1146/annurev-immunol-032414-112043.
Fachbücher mit vielen Informationen zum Thema "Immunsystem und Krebs" sind zum Beispiel die folgenden:
Murphy K, Travers P, Walport M. Janeway Immunologie. 7. Auflage 2009. Spektrum Akademischer Verlag Heidelberg.
Die aktuelle englischsprachige Fassung ist von 2017: Murphy K, Weaver C. Janeway's immunobiology. 9th edition 2017. Garland Science London & New York.
Weinberg RA. The biology of cancer. 2nd edition 2014. Garland Science London & New York.
Das Deutsche Krebsforschungszentrum (DKFZ) informiert zur Forschung zum Thema "Tumorimmunologie" auf seinen Internetseiten unter www.dkfz.de, Reiter "Forschung", Stichwort "Forschungsschwerpunkte", "Tumorimmunologie".