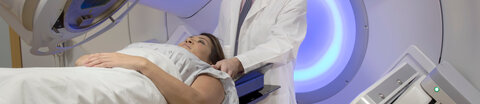
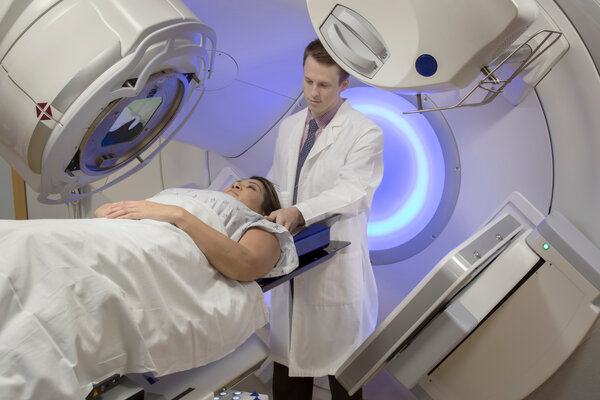
- Es gibt viele verschiedene Bestrahlungstechniken. Welche angewendet wird, hängt vom Tumor und der individuellen Situation ab.
- Eine Strahlentherapie ist dank vielen technischen Weiterentwicklungen heute viel schonender für das gesunde Gewebe. Schwere Nebenwirkungen sind dadurch seltener.
- Dieser Text erklärt die wichtigsten Techniken und Fachbegriffe zum Thema Bestrahlung.
Strahlentherapie: Welche Technik wird derzeit als Standard verwendet?
Zum Weiterlesen
Mit welcher Technik man bestrahlt wird, ist von der Art der Tumorerkrankung und der individuellen Krankheitssituation abhängig. Manche Verfahren kommen nur für wenige Patienten infrage, andere werden noch in Studien erprobt. Die klassische Bestrahlung, die sogenannte perkutane Strahlentherapie, wird schon sehr lange eingesetzt. Sie gilt trotzdem immer noch als eine Art Standard: Etwa fünfundneunzig von hundert Patientinnen und Patienten, die im Laufe ihrer Krebserkrankung eine Bestrahlung erhalten, werden so behandelt.
Bei dieser Behandlungsform werden Strahlen mithilfe eines Linearbeschleunigers erzeugt. Als Patientin oder Patient liegt man auf einer Liege unter dem Bestrahlungsgerät. Die Strahlen dringen von außen durch den Körper – von daher der Name: perkutan bedeutet "durch die Haut".
Mit moderner Technik gesundes Gewebe schonen
Bei der Bestrahlung eines Tumors oder einer Metastase stellt die Mitbestrahlung von gesundem Gewebe ein grundsätzliches Problem dar: Die höchste Strahlendosis soll ja den Tumor treffen und die Tumorzellen schädigen und nicht die Haut. Weiterentwicklungen der Strahlentherapie haben daher vor allem ein Ziel: Gesundes Gewebe soll besser geschont werden.
Dies lässt sich zum Beispiel durch die Anordnung der sogenannten Bestrahlungsfelder erreichen. Was heißt das? Ein Bestrahlungsfeld ist die Fläche, die bestrahlt wird, wenn die Strahlen aus einer bestimmten Richtung auf den Körper treffen. Moderne Bestrahlungstechniken verwenden mehrere Bestrahlungsfelder, und die Strahlen treffen aus verschiedenen Richtungen auf den Körper. Es gilt: Dort, wo sich die Strahlen aus den verschiedenen Richtungen kreuzen, ist die Dosis am höchsten.
Diesen Effekt macht man sich bei der heute üblichen sogenannten "konformalen Mehrfelderbestrahlung" zunutze. Obwohl mit einer geringeren Strahlendosis pro Einstrahlrichtung gearbeitet wird, um das gesunde Gewebe zu schonen, wird im Tumor selbst eine gleichmäßig hohe Strahlendosis erreicht.
Hinzu kommt: Mithilfe von Strahlenblenden innerhalb des Bestrahlungsgerätes können heute Strahlenfelder unterschiedlicher Formen erzeugt werden: So werden sie der Form des jeweiligen Tumors angepasst und gesundes Gewebe wird geschont.
Einzelne Strahlentherapietechniken: Stellenwert, Kostenübernahme
Welche Behandlung kommt infrage?
Nicht jede Strahlentherapie-Technik ist in jeder Erkrankungssituation möglich oder sinnvoll. Bei der Frage, welche Therapie für eine Patientin oder einen Patienten am geeignetsten ist, berücksichtigen Ärzte die persönliche Situation der Betroffenen. Sie greifen dabei auch auf Erfahrungswerte und Statistiken aus klinischen Studien zurück. In den medizinischen Leitlinien der Fachgesellschaften wird der Stellenwert einer Behandlung für eine bestimmte Tumorerkrankung in einem bestimmten Stadium erläutert. Welche Behandlungen bei welcher Tumorerkrankung möglich und sinnvoll sind, erläutern die Texte des Krebsinformationsdienstes unter Krebsarten.
Was zahlt die Krankenkasse und was nicht?

Bild: © Halfpoint, Thinkstock
Die gesetzlichen Krankenversicherungen übernehmen die Kosten für die Untersuchungen und die Behandlung einer Erkrankung, sofern diese "ausreichend, zweckmäßig und wirtschaftlich" sind und sofern die Untersuchungen oder Behandlungen nicht überflüssig sind, also mehr gemacht wird, als notwendig ist. Bei der Frage, welche Leistungen bezahlt werden und welche nicht, sind die Kassen an gesetzliche Vorgaben gebunden. Für die privaten Krankenversicherungen gilt der jeweilige Versicherungsvertrag.
Nicht alle unter Lexikon: Grundbegriffe und Lexikon: Weiterentwicklungen aufgeführten Bestrahlungstechniken sind bereits "Kassenleistung". Und nicht alle Leistungen sind überall in Deutschland verfügbar: Manche technische Neuerungen benötigen teure Geräte oder ganze Anlagen, die viel Platz beanspruchen und sehr viel Energie benötigen und deshalb nur an spezialisierten Zentren vorhanden sind.
Auch ist nicht immer abschließend geklärt, ob mögliche Vorteile einer Behandlung die auch vorhandenen Risiken aufwiegen oder nicht. Das bedeutet: Einige der Weiterentwicklungen stehen daher nur Betroffenen in einer ganz bestimmten Krankheitssituation und auch nur im Rahmen klinischer Studien zur Verfügung.
Wer hilft weiter?
Wenn Sie als Betroffener oder Angehöriger Fragen zu einer bestimmten Bestrahlungsmethode haben, wenden Sie sich zunächst an die behandelnden Ärzte. Diese können am besten einschätzen, ob eine Methode in einer bestimmten Erkrankungssituation sinnvoll und angemessen ist. Die Krankenkassen können Auskunft darüber geben, wann die Kosten für eine Therapie übernommen werden können und wann nicht. Als weiterer Ansprechpartner steht Ihnen die Unabhängige Patientenberatung Deutschland zur Verfügung. Kontaktmöglichkeiten finden Sie auf deren Internetseite unter www.patientenberatung.de.
Fragen zu Krebs? Wir sind für Sie da!
Sie haben Fragen zur Strahlenbehandlung? Wir stehen Ihnen gerne am Telefon oder per E-Mail zur Verfügung: Unter 0800 - 420 30 40 beantworten wir täglich von 8.00 bis 20.00 Uhr Ihre Fragen. Oder Sie schreiben uns eine E-Mail an krebsinformationsdienst@dkfz.de (beim Klicken öffnet sich ein gesichertes Kontaktformular).
Lexikon: Grundbegriffe der Strahlenbehandlung
Wellen und Teilchen
Atome: kleine Bausteine der Materie; Atome bestehen aus einem Kern und einer Hülle
Elektronen: Negativ geladene Elementarteilchen in der Hülle eines Atoms
Positronen: Positiv geladene "Gegenstücke" der Elektronen
Neutronen: Ungeladene Teilchen im Kern eines Atoms
Protonen: Positiv geladene Teilchen im Kern eines Atoms
Ionen: "geladene" Atome oder Moleküle mit einem Überschuss oder Mangel an Elektronen
Photonen: elektromagnetische Wellen bestehen aus kleinen "Energieeinheiten", den Photonen
Hadronen: Überbegriff für Teilchen, die von starker Wechselwirkung zusammengehalten werden. Zu ihnen gehören unter anderem:
Pionen: Instabile Teilchen, die positiv, negativ oder ungeladen sein können
Schwerionen: Ionen ab einer bestimmten Masse
Einen Überblick über Grundbegriffe der Physik bietet die Deutsche Physikalische Gesellschaft (DPG) auf www.weltderphysik.de.
Bestrahlung, Strahlentherapie: Eine Bestrahlung ist eine Behandlung mithilfe ionisierender Strahlen, zum Beispiel ultraharten Röntgenstrahlen oder radioaktiven Strahlen. Die Bestrahlung bei Krebs soll Tumorzellen zerstören. Sie kann die alleinige Behandlung sein – oder sie kann mit anderen Therapieformen kombiniert werden, wie einer Chemotherapie oder Operation. Häufig gestellte Fragen zur Strahlentherapie und Nuklearmedizin beantwortet der Krebsinformationsdienst in einem eigenen Text.
Bestrahlungsfeld: Der Teil der Körperoberfläche, durch den die Strahlen in den Körper eindringen, wird Bestrahlungsfeld genannt. Bei vielen Betroffenen werden mehrere Bestrahlungsfelder auf der Haut eingezeichnet: Der Tumor wird üblicherweise aus unterschiedlichen Richtungen so bestrahlt, dass sich die Strahlen im Krebsgewebe konzentrieren. Gesundes Gewebe wird so geschont: Es wird möglichst nur aus einer Richtung mitbestrahlt. Mehr zum Thema finden Sie im Kapitel Strahlentherapie: Anwendungen und Nebenwirkungen.
Brachytherapie: Die Brachytherapie ist eine Bestrahlung aus nächster Nähe: Eine radioaktive Substanz wird in eine Körperhöhle oder direkt ins Gewebe eingebracht und bestrahlt von dort aus den Tumor. In der Regel wird die Substanz direkt nach der Behandlungssitzung wieder entfernt, sie kann aber auch länger im Gewebe verbleiben. Wie genau die Brachytherapie abläuft, wird im Kapitel Strahlentherapie: Anwendungen und Nebenwirkungen erklärt. Welche weiteren Begriffe sind wichtig, wenn es um die Brachytherapie geht?
- Applikator: Ein Applikator ist eine leere Hülse oder ein Schlauch, der vor der Brachytherapie in den Körper eingebracht wird. Ob die Applikatoren richtig sitzen, prüfen die Ärzte vor der Therapie, zum Beispiel mit einer Computertomographie-Aufnahme. Anschließend können sie eine strahlende Substanz in den Applikator einbringen.
- Afterloading-Verfahren: Beim sogenannten Afterloading-Verfahren wird die radioaktive Substanz ferngesteuert in den Applikator eingeführt. Dies hat den Vorteil, dass das medizinische Personal sich währenddessen außerhalb des Bestrahlungsraums aufhalten kann und nichts von der radioaktiven Strahlung abbekommt. Dieser Schutz ist wichtig: Da das Personal sonst täglich Strahlung ausgesetzt würde, wäre die Belastung für die Mitarbeiter langfristig ungleich höher als für die einzelnen Patienten.
- Intrakavitäre Therapie: So nennt man eine Brachytherapie, bei der die Applikatoren und die strahlende Substanz in eine natürliche Körperhöhle eingeführt werden, zum Beispiel in die Gebärmutter, Scheide, Harnblase, die Speiseröhre, Gallengänge oder Bronchien.
- Interstitielle Therapie: Hierbei werden Applikatoren und strahlende Substanz direkt in den Tumor oder das umliegende Gewebe eingebracht. Bei der sogenannten Seed-Implantation werden sehr kleine Metallhülsen verwendet. Sie enthalten eine radioaktive Strahlenquelle, die über einen gewissen Zeitraum Strahlung mit geringer Reichweite abgibt. Die Strahlung der Seeds nimmt ständig ab, bis gar keine Strahlung mehr von ihnen ausgeht. Eine operative Entfernung ist deshalb nicht zwingend erforderlich.
- Kontakttherapie: Zur Bestrahlung der Haut oder Schleimhaut wird die strahlende Substanz in einem Applikator direkt auf die zu bestrahlende Fläche aufgebracht. Der Applikator besteht oft aus formbarem Material, das der Kontaktfläche angepasst werden kann.
Dosis, Strahlendosis, Energiedosis: Die Strahlendosis ist die Menge an Energie, die bei der Strahlenbehandlung auf den Körper einwirkt. Genauer spricht man von Energiedosis: Das ist die Strahlenmenge, die pro Kilogramm Körpergewebe aufgenommen wird. Sie wird in der Einheit Gray (Abkürzung Gy) angegeben. Je höher die Strahlendosis, desto wirksamer ist die Behandlung gegen den Tumor. Allerdings steigt auch das Risiko für schwerwiegende Nebenwirkungen und für chronische Strahlenfolgen.
- Fraktionierung, fraktionierte Bestrahlung: Eine Strahlentherapie kann aus einer einzigen Behandlungssitzung bestehen. Bei den meisten Patientinnen und Patienten wird die Gesamtstrahlendosis jedoch auf mehrere Sitzungen verteilt. Ärzte sprechen von einer fraktionierten Bestrahlung. Der Vorteil: Die Belastung für das gesunde Gewebe ist nicht so hoch, es kann sich zwischen den Sitzungen besser erholen – Krebsgewebe gelingt dies nicht so schnell.
Radioaktive Strahlung: Ionisierende Strahlung entsteht unter anderem bei dem Zerfall instabiler Atomkerne: Zerfallen diese, wird Energie in Form von Strahlung frei. Der Kernzerfall wird deshalb auch als radioaktiver Zerfall bezeichnet, die frei gesetzte Strahlung als radioaktive Strahlung.
- Alpha-, Beta-, Gamma-Strahlen: Beim Zerfall von Atomkernen können unterschiedliche Strahlenarten frei werden. Ausführlichere Informationen zum Thema bietet der Text Radioaktivität und Röntgenstrahlen.
- Radionuklidtherapie: Die instabilen Atomkerne nennt man Radionuklide, übersetzt "strahlende Kerne". Bei der Radionuklidtherapie erhalten Patienten solche radioaktiven Stoffe als Medikament. Die Radionuklide werden von Tumorzellen aufgenommen oder binden gezielt an diese und bestrahlen sie direkt. Gesundes Gewebe hat entweder einen anderen Stoffwechsel als die Krebszellen und nimmt daher weniger Radionuklide auf oder aber die Zellen weisen nicht die Bindungsstellen auf, an die die Radionuklide andocken. Mehr zur Radionuklidtherapie finden Sie im Kapitel Nuklearmedizin: Durchführung und Nebenwirkungen.
Teletherapie, perkutane Bestrahlung: Bei dieser "klassischen" Bestrahlung liegt die Bestrahlungsquelle in einiger Entfernung zum Körper. Als Patient liegt man auf einer Liege unter dem Bestrahlungsgerät. Man wird von außen bestrahlt, "perkutan", also "durch die Haut". Bei den heute gängigen Verfahren wird die Strahlung in der Regel mithilfe eines Linearbeschleuniger erzeugt, es gibt jedoch noch weitere Möglichkeiten:
- Linearbeschleuniger: Mit einem Elektronen-Linearbeschleuniger werden elektrisch geladene Teilchen, Elektronen, erzeugt und auf nahezu Lichtgeschwindigkeit beschleunigt. Für die Strahlenbehandlung von tiefer liegenden Tumoren sind die so erzeugten Elektronenstrahlen allerdings weniger geeignet, weil sie nicht tief in den Körper eindringen. Daher werden die Elektronen üblicherweise innerhalb des Gerätes abgebremst. Die frei werdende ultraharte Röntgenbremsstrahlung, Photonenstrahlung, dringt tiefer in den Körper ein und kann so für die Strahlentherapie von Tumoren im Körperinnern genutzt werden.
- Röntgentherapie: Neben der üblichen ultraharten Röntgenstrahlung im Megavolt-Bereich gibt es auch Behandlungen mit Röntgenstrahlung niedrigerer Spannung. Man unterscheidet Röntgen-Weichstrahltherapie und Hartstrahltherapie voneinander, je nachdem, wie hoch die angelegte Spannung ist. Die Bestrahlung mit Röntgenstrahlung im Kilovolt-Bereich wird aufgrund der geringen Eindringtiefe nur für oberflächliche Hauttumoren angewendet, zum Beispiel das Basalzellkarzinom.
- Telegammatherapie, Telekobaltgerät: Auch zur Teletherapie gerechnet wird die sogenannte Telegammatherapie. Sie nutzt Gammastrahlung, die beim Zerfall radioaktiver Substanzen frei wird. Man verwendet zum Beispiel Kobalt 60 (60Co). Die Photonenstrahlung wird durch mehrere Blenden auf das Ziel eingestellt. Ebenfalls frei werdende Alpha- und Betastrahlung wird durch einen dicken Bleimantel abgeschirmt. Weil die Geräte dadurch sehr klobig aussahen, wurden sie umgangssprachlich auch "Kobaltkanonen" genannt. Inzwischen sind sie zumindest in Deutschland überwiegend durch Linearbeschleuniger ersetzt: Bei diesen ist die Strahlung besser steuerbar, und es fallen keine radioaktiven Abfallprodukte an. Heute kommt Kobalt vor allem noch in Spezialgeräten zur stereotaktischen Bestrahlung von Hirntumoren und Hirnmetastasen zum Einsatz, als sogenanntes Gamma KnifeTM. Bei der Bestrahlung von Tumoren im Kopf-Hals-Bereich werden außerdem Cäsium-137 (137Cs)-Bestrahlungsanlagen verwendet.
Lexikon: Technische Weiterentwicklungen der Teletherapie
Das meistgenutzte Verfahren ist die Bestrahlung von außen, die sogenannte perkutane Teletherapie. Als Standardtechnik innerhalb der perkutanen Strahlenbehandlung gilt die konformale Mehrfelderbestrahlung. Inzwischen gibt es viele verschiedene technische Weiterentwicklungen. Sie haben im Wesentlichen ein Ziel: die Strahlenwirkung im Tumor zu erhöhen und gesundes Gewebe zu schonen. Viele der verschiedenen Techniken können miteinander kombiniert werden.
Bewegungsbestrahlung, Rotationsbestrahlung
Bei der Bewegungsbestrahlung ist die Strahlenquelle nicht fest stehend. Der Strahlerkopf bewegt sich vielmehr in einem Bogen oder kreisförmig um die Patientenliege. Entsprechend spricht man von einer Pendelbestrahlung beziehungsweise Rotationsbestrahlung. Dadurch ändert sich der Einstrahlwinkel. Der Tumor wird fortlaufend bestrahlt: Dort kreuzen sich alle Strahlen. Es wird jedoch immer nur kurzzeitig ein anderes Stück Haut und ein anderer Bereich des gesunden Gewebes mit bestrahlt. Die Strahlenbelastung wird so vermindert.
Ganzkörperbestrahlung
Bei der Ganzkörperbestrahlung wird der ganze Körper einschließlich der Haut bestrahlt. Diese Form der Bestrahlung kommt zum Beispiel bei einigen Leukämie- oder Lymphomformen vor einer Knochenmark- oder Bluststammzelltransplantation zur Anwendung.
IGRT: Bildgesteuerte Strahlentherapie
Die bildgesteuerte Strahlentherapie (Image Guided Radiotherapy, IGRT) ermöglicht es Ärzten, direkt vor oder während der Bestrahlung noch einmal die genaue Lage des Tumors zu überprüfen. Dies ist mit bildgebenden Verfahren möglich, zum Beispiel mithilfe einer Computertomographie. Die Bilder werden an das Bestrahlungsgerät übertragen, und eventuelle Lageverschiebungen des Tumors können sofort berücksichtigt werden. Gegebenenfalls bekommt man dazu vor der Behandlung kleine Positionierungsmarker aus Gold eingesetzt. Die Bestrahlung wird durch dieses Verfahren genauer, und besonders sensible Organe in der Nähe können geschont werden.
IMRT: Intensitätsmodulierte Strahlentherapie
Bei der intensitätsmodulierten Radiotherapie (IMRT) wird nicht nur die Form der Bestrahlungsfelder an die des Tumors angepasst. Jedes einzelne Bestrahlungsfeld wird noch einmal in kleinere Bereiche aufgeteilt. Jedes dieser Segmente kann mit einer unterschiedlich hohen Dosis bestrahlt werden. Dadurch kann strahlenempfindliches Gewebe im Strahlengang besser geschont und trotzdem im Tumor eine gleichmäßig hohe Strahlendosis erreicht werden. Die Therapieplanung ist bei der IMRT jedoch deutlich aufwendiger als beim Standardverfahren.
IMRT und IGRT: Weiterentwicklungen
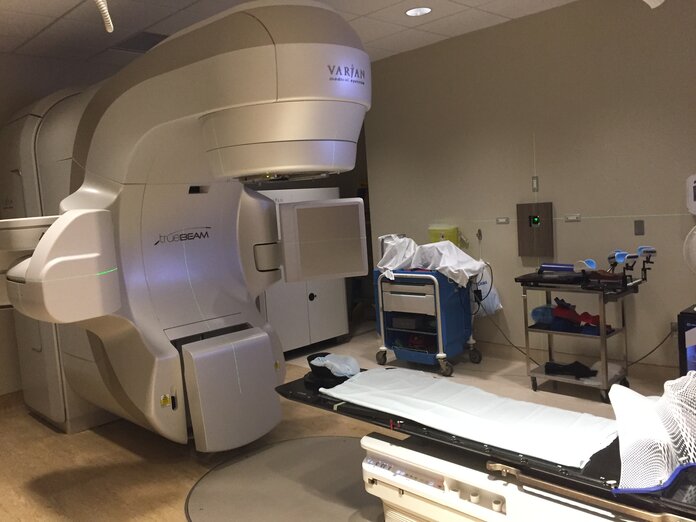
Bild: Michael Goodyear /Wikimedia Commons
Die IMRT kann mit der IGRT kombiniert werden. Für die intensitätsmodulierte Strahlentherapie in Kombination mit der Bildsteuerung gibt es verschiedene technische Weiterentwicklungen. Diese werden teilweise noch in Studien erprobt. Langfristige Vorteile und Risiken sind noch nicht immer im Einzelnen erforscht.
Dynamisch adaptierte Radiotherapie (DART/ART): Die adaptierte Radiotherapie ist eine Verfeinerung der IMRT in Kombination mit einer Bildsteuerung (IGRT). Kontinuierlich werden CT-Bilder aufgenommen und mit dem Bestrahlungsplan abgeglichen. Selbst Darmbewegungen oder Atembewegungen werden unter laufender Bestrahlung berücksichtigt. In kürzester Zeit kann die Dosis überprüft und angepasst werden.
Tomotherapie: Bei der Tomotherapie rotiert die Strahlenquelle spiralförmig um den Körper. Mit der Tomotherapie können sehr lange Bestrahlungsfelder in einem Stück bestrahlt werden. Im Bestrahlungsgerät selbst ist ein Computertomograph eingebaut, der für die Bildgebung vor jeder Bestrahlung genutzt werden kann.
Intensitätsmodulierte Rotationsbestrahlung (IMAT/VMAT): Bei der intensitätsmodulierten Strahlentherapie bewegt sich die Strahlenquelle um die Patientenliege. Größe und Form des Bestrahlungsfeldes und die Rotationsgeschwindigkeit können während der Behandlung angepasst werden. Kann auch die Strahlendosis unter der Bestrahlung verändert werden, spricht man von einer volumetrisch modulierten Rotationsbestrahlung (Volumetric modulated Arc Therapy, VMAT). Im Gerät ist üblicherweise ein Computertomograph integriert: Die CT-Bilder ermöglichen es den Behandlern, unmittelbar vor der Bestrahlung noch einmal die Lage des Patienten überprüfen und die Strahlen noch genauer auf den Tumor ausrichten.
Intraoperative Radiotherapie (IORT)
Wird ein Tumor chirurgisch entfernt, kann das Randgebiet schon während der Operation bestrahlt werden. Eine solche Bestrahlung ergänzt häufig eine reguläre Bestrahlung "durch die Haut". Die Bestrahlung während einer Operation hat zwei Vorteile: Zum einen ist direkt sichtbar, wo der herausoperierte Tumor sich befunden hat. Zum anderen kann umliegendes Gewebe besser geschont werden: Die Chirurgen können empfindliche Organe vorübergehend aus dem Weg schieben oder mithilfe von Bleimatten abdecken und so vor den Strahlen schützen. Die IORT wird vor allem dann eingesetzt, wenn zu befürchten ist, dass der Tumor an derselben Stelle zurückkehren könnte. Sie wird vor allem im Bauchraum angewendet, aber auch bei Brustkrebs oder Tumoren im Beckenbereich. Sie ist kein Standardverfahren. Groß angelegte Studien zu diesem Verfahren fehlen bisher.
IORT mit Elektronenstrahlen: Meist werden Elektronenstrahlen verwendet, die eine geringere Reichweite haben als Photonenstrahlen. Die Strahlen müssen ja keine äußeren Haut- und Gewebeschichten mehr durchdringen und können direkt auf den Tumor oder das Tumorbett gerichtet werden.
IORT mit Röntgenstrahlen: Eine andere Möglichkeit ist die Bestrahlung mit niedrigenergetischer Röntgenstrahlung.
IORT als Brachytherapie: Oder es kann intraoperativ eine Brachytherapie durchgeführt werden: In die Operationshöhle wird eine Matte ("Flab") mit dünnen Röhrchen gelegt, in die mittels Afterloading-Verfahren ein Radionuklid eingeführt wird. Der Flab kann vor dem Ende der Operation wieder entfernt werden oder vorübergehend im Körper verbleiben.
Ionenstrahltherapie und andere Teilchenstrahlung
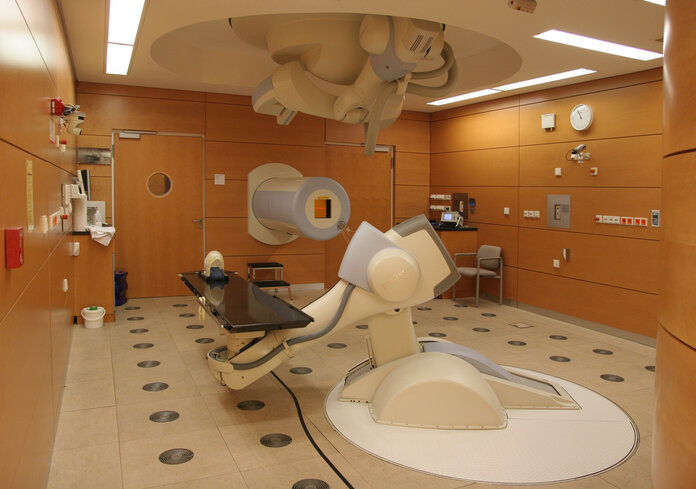
Bild: Armin Kübelbeck/Wikimedia Commons
Die Ionenstrahltherapie ist eine besondere Form der Strahlentherapie. Anders als die klassische Strahlentherapie mit Photonen nutzt die Ionenstrahltherapie keine elektromagnetischen Wellen für die Bestrahlung eines Tumors, sondern geladene Teilchen. In der Praxis finden vor allem die Protonen- und Schwerionenbestrahlung Anwendung. Protonen sind positiv geladene Wasserstoffatomkerne. Schwerionen sind positiv geladene Kerne von Atomen mit größerer Masse als Wasserstoff, zum Beispiel von Kohlenstoff-, Helium- oder Sauerstoffatomen.
Ionenstrahlen können zielgenau auf den Tumor gelenkt werden. Sie belasten die Haut und das umliegende Gewebe weniger, da sie ihre Energie erst in der Tiefe abgeben, also im Tumor selbst. Dadurch kann der Tumor mit einer höheren Dosis bestrahlt werden, ohne dass das Nebenwirkungsrisiko für gesundes Gewebe im Strahlengang im gleichen Maße zunimmt. Auch sehr tief liegende Tumoren können erreicht werden.
Eine Ionenstrahltherapie kommt allerdings nur für bestimmte Tumoren infrage. Auch ist eine Ionenstrahltherapie technisch sehr aufwendig. Die hierfür benötigten Geräte gibt es daher in Deutschland und weltweit nur an wenigen spezialisierten Krebszentren.
Radiochemotherapie
Die Radiochemotherapie kombiniert zwei Krebsbehandlungen: die Bestrahlung und die Chemotherapie. Die beiden Methoden werden entweder zeitgleich oder nacheinander angewendet. Man erhofft sich davon eine stärkere Wirkung auf den Tumor: Durch die Chemotherapie vorgeschädigte Tumorzellen sind zum Beispiel anfälliger für die Wirkung der Strahlen. Welche Chemotherapie-Medikamente begleitend zur Bestrahlung infrage kommen, ist davon abhängig, welchen Tumor man hat.
Stereotaktische Bestrahlung: Radiochirurgie, Gamma KnifeTM, CyberknifeTM
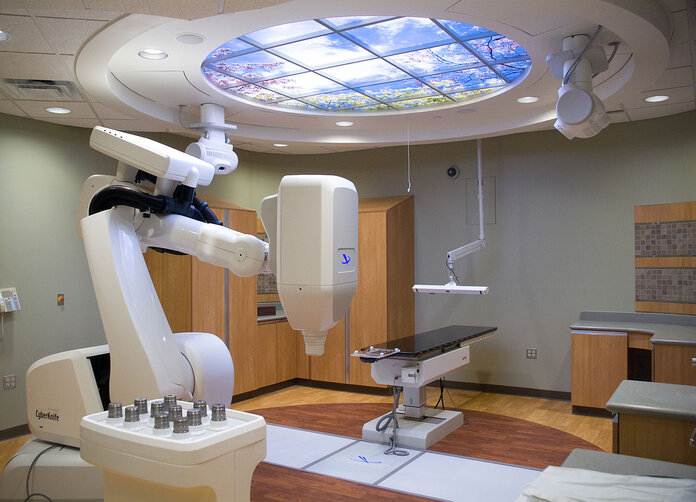
Bild: Saginaw Future/Wikimedia Commons
Bei der stereotaktischen Bestrahlung wird ein kleiner, gut abgegrenzter Tumor mit einer hohen Strahlendosis zielgenau bestrahlt. Man spricht daher auch von Hochpräzisionsstrahlentherapie. Der Vorteil der stereotaktischen Bestrahlung: Durch die sehr genaue Bestrahlung kann strahlenempfindliches Gewebe in unmittelbarer Nähe des Tumors bestmöglich geschont werden. Anhand der Zahl der Bestrahlungssitzungen unterscheidet man die sogenannte Radiochirurgie von der fraktionierten stereotaktischen Radiotherapie. Eine Unterform ist die perkutane stereotaktische Bestrahlung: Hier ist auch die Verwendung der Markennamen einzelner Gerätesysteme üblich.
Radiochirurgie oder Strahlenchirurgie: Bei der Radiochirurgie wird der Tumor in der Regel "einzeitig", also nur einmal mit einer einzelnen hohen gewebezerstörenden Dosis bestrahlt. Die Radiochirurgie wird vor allem zur Behandlung von Hirnmetastasen angewendet. Sie kann auch dann eingesetzt werden, wenn die Operation durch einen Neurochirurgen nicht möglich ist. Auch bei einigen klar abgrenzbaren, meist gutartigen Hirntumoren kommen stereotaktische Bestrahlungen infrage. Wichtig ist, dass man sich während der Behandlung nicht bewegt: Für eine Bestrahlung im Kopfbereich erhalten die meisten Patienten daher eine eigens angefertigte Maske. Oder man bekommt vorab einen sogenannten stereotaktischen Rahmen, der unter lokaler Betäubung vorsichtig am Kopf fixiert wird. So wird sichergestellt, dass sich der Kopf wirklich in der vorgesehenen Position befindet.
Fraktionierte stereotaktische Radiotherapie (FSRT, SRT): Unter einer fraktionierten Bestrahlung versteht man die Aufteilung der Gesamtstrahlendosis auf mehrere Sitzungen. Die Behandlung erstreckt sich über mehrere Tage bis Wochen.
Perkutane stereotaktische Behandlung, Gamma KnifeTM, CyberknifeTM: Es wird entweder Gammastrahlung eingesetzt, die von einer radioaktiven Substanz, meist Kobalt-60, freigesetzt wird (Markenname des Systems: Gamma KnifeTM). Oder es wird mit ultraharter Röntgenstrahlung bestrahlt (Photonenbestrahlung), die von einem Linearbeschleuniger erzeugt wird. Eine Sonderform stellt das sogenannte CyberknifeTM-System dar: Hier ist ein kompakter Linearbeschleuniger auf einen Roboterarm montiert, der um die Behandlungsliege bewegt werden kann. Bei Bestrahlungen im Kopfbereich ist es bei dieser Methode nicht notwendig, den Kopf in einem stereotaktischen Rahmen zu fixieren.
Interstitielle stereotaktische Bestrahlung: Durch kleine Hohlnadeln wird eine radioaktive Substanz in den Tumor eingeführt. Diese sogenannten Seeds können nach der Behandlung wieder entfernt werden oder aber dauerhaft im Körper verbleiben. Mit der Zeit nimmt die Strahlung ab.
Extrakranielle Stereotaxie: Auch außerhalb des Kopfbereiches kann die Radiochirurgie angewendet werden: zum Beispiel bei Lebermetastasen oder Lungenmetastasen oder bestimmten Formen von Lungenkrebs im Frühstadium.
Quellen und Links für Interessierte und Fachkreise
Im Folgenden finden Sie eine Auswahl an hilfreichen Links zum Weiterlesen und Quellen, die für die Erstellung dieses Textes genutzt wurden.
Fachgesellschaften und Forschungseinrichtungen
Das Bundesamt für Strahlenschutz (BfS) ist eine wissenschaftlich-technische Bundesoberbehörde. Es ist dem Bundesministerium für Umwelt, Naturschutz, Bau und Reaktorsicherheit (BMUB) unterstellt. Das BfS beschäftigt sich mit den Themen elektromagnetische Felder, optische Strahlung, ionisierende Strahlung, Kerntechnik und nukleare Entsorgung. Es ist für den Schutz der Bevölkerung und der Umwelt vor Schäden durch ionisierende und nicht ionisierende Strahlung zuständig.
Informationen zu ionisierende Strahlung sind auf dieser Seite zusammengestellt: www.bfs.de/DE/themen/ion/ion_node.html. Unter dem Menüpunkt "Anwendungen in der Medizin" finden Sie unter anderem Informationen zur Strahlentherapie.
Die Deutsche Gesellschaft für Radioonkologie e. V. (DEGRO) ist eine wissenschaftliche Fachgesellschaft von Ärzten, Medizinphysikern und Strahlenbiologen, die sich mit der Strahlenbehandlung von Krebs beschäftigen. Die DEGRO fördert wissenschaftliche Forschung zum Thema und kümmert sich um die Umsetzung der wissenschaftlichen Erkenntnisse in der Patientenbehandlung.
Auf der Internetseite der DEGRO, www.degro.org, finden Sie Leitlinien zur Strahlentherapie bei verschiedenen Tumorarten sowie zur unterstützenden Behandlung von Strahlenschäden.
Die Deutsche Gesellschaft für Nuklearmedizin e. V. (DGN) fördert als wissenschaftliche Fachgesellschaft Forschung zu nuklearmedizinischen Untersuchungen und Behandlungen. Auf ihrer Internetseite, www.nuklearmedizin.de, hat sie Leitlinien zu Themen wie Szintigraphie, PET oder zur Radionuklidtherapie bei verschiedenen Tumorarten veröffentlicht. Für Patienten gibt es eine Klinik-Suchfunktion, um nuklearmedizinische Abteilungen und Praxen in der Nähe des eigenen Wohnorts zu finden.
Das Institut für Strahlenbiologie (ISB) des Helmholtz-Zentrums München forscht zu den Auswirkungen ionisierender Strahlung auf den Menschen sowie zur Strahlentherapie von Tumoren. Einen Überblick über die Forschungsschwerpunkte und Publikationen des Instituts bietet die Internetseite des ISB: www.helmholtz-muenchen.de/isb/index.html.
Das Deutsche Krebsforschungszentrum (DKFZ) forscht auch zu den Themen Strahlentherapie und Nuklearmedizin. Unter www.dkfz.de/de/forschung/schwerpunkte/fsp-e.php informiert der Forschungsschwerpunkt "Bildgebung und Radioonkologie" im Krebsforschungszentrum über seine Aufgaben und Ergebnisse. Gemeinsam mit der Radiologischen Universitätsklinik Heidelberg setzt der Forschungsschwerpunkt neue Entwicklungen zum Nutzen von Patienten in die Praxis um. Auf der Internetseite der radiologischen Klinik finden Sie unter anderem Informationen über das Heidelberger Ionenstrahl-Therapiezentrum (HIT): https://www.klinikum.uni-heidelberg.de/radiologische-klinik.
Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWIG, www.iqwig.de) ist eine Einrichtung der privaten und gemeinnützigen Stiftung für Qualität und Wirtschaftlichkeit im Gesundheitswesen. Das IQWIG soll helfen, evidenzbasierte Entscheidungen in Gesundheitsfragen zu treffen. Die Internetseite www.gesundheitsinformation.de informiert die Öffentlichkeit über Gesundheitsfragen. Über die Stichwortsuche der Suchmaschine der Seite findet man auch Informationen zum Thema "Strahlentherapie", "Bestrahlung" oder "Brachytherapie".
Leitlinien und Stellungnahmen verschiedener Fachgesellschaften
Deutsche Gesellschaft für Nuklearmedizin. DGN-Handlungsempfehlung (S1-Leitlinie). Radioiodtherapie beim differenzierten Schilddrüsenkarzinom. 10/2015.
Deutsche Gesellschaft für Nuklearmedizin. DGN-Handlungsempfehlung (S1-Leitlinie). Radionuklidtherapie von Knochenmetastasen mittels Radium-223. 10/2015.
Deutsche Gesellschaft für Nuklearmedizin. Fischer M. Leitlinie für die Radionuklidtherapie bei schmerzhaften Knochenmetastasen.
Die Leitlinien der Deutschen Gesellschaft für Nuklearmedizin (DGN), zum Beispiel zur Radionuklidtherapie bei verschiedenen Indikationen, sind auf der Internetseite der DGN abrufbar unter www.nuklearmedizin.de/leistungen/leitlinien/leitlinien.php?navId=53.
DEGRO. S2-Leitlinie: Supportive Maßnahmen in der Radioonkologie. 2015.
DEGRO. Leitlinie zur Strahlentherapie mit fluenzmodulierten Feldern (IMRT). 2005.
Informationen zu den Leitlinien der Deutschen Gesellschaft für Radioonkologie (DEGRO) sind abrufbar auf der Internetseite https://www.degro.org/degro/leitlinien/.
Arbeitsgemeinschaft Pädiatrische Radioonkologie (APRO). Positionspapier der GPOH, DEGRO und APRO zur Partikeltherapie bei Kindern. 2011.
Diese und weitere Stellungnahmen und Positionspapiere der DEGRO sind im PDF-Format von dieser Seite herunterladbar: https://www.degro.org/degro/positionspapiere_stellungnahmen/.
Leitlinienprogramm Onkologie
Arbeitsgemeinschaft Supportive Maßnahmen in der Onkologie, Rehabilitation und Sozialmedizin der Deutschen Krebsgesellschaft (ASORS). S3-Leitlinie: Supportive Therapie bei onkologischen PatientInnen. 2016. Internet: https://www.leitlinienprogramm-onkologie.de/leitlinien/supportive-therapie.
Arbeitsgemeinschaft Gynäkologische Onkologie (AGO)
AGO. Diagnostik und Therapie primärer und metastasierter Mammakarzinome. Adjuvante Strahlentherapie. Guidelines Breast. 2016.1D. Internet: www.ago-online.de/de/infothek-fuer-aerzte/leitlinienempfehlungen/mamma
American Society of Clinical Oncology (ASCO) / American Society for Radiation Oncology (ASTRO) / Society of Surgical Oncologists (SSO)
ASCO-ASTRO-SSO Clinical Practice Guideline: Recht A, Somerfield MR et al. Postmastectomy Radiotherapy: An American Society of Clinical Oncology, American Society for Radiation Oncology, and Society of Surgical Oncology Focused Guideline Update. J Clin Oncol. 2016 Sep 19. pii: JCO691188. [Epub ahead of print]. Internet: http://ascopubs.org/doi/pdf/10.1200/JCO.2016.69.1188
Deutsche Gesellschaft für Ernährungsmedizin (DGEM)
Arends J, Bertz H, Bischoff S.C, Fietkau R, Herrmann H.J, Holm E, Horneber M, Hütterer E, Körber J, Schmid I, und das DGEM Steering Committee. S3-Leitline der Deutschen Gesellschaft für Ernährungsmedizin e. V. (DGEM) in Kooperation mit der Deutschen Gesellschaft für Hämatologie und Onkologie e. V. (DGHO), der Arbeitsgemeinschaft "Supportive Maßnahmen in der Onkologie, Rehabilitation und Sozialmedizin" der Deutschen Krebsgesellschaft (ASORS) und der Österreichischen Arbeitsgemeinschaft für klinische Ernährung (AKE). Klinische Ernährung in der Onkologie. Aktuel Ernahrungsmed 2015; 40: e1–e74, DOI 10.1055/s-0035-1552741. Internet: www.awmf.org/leitlinien/detail/ll/073-006.html
Empfehlungen zum Strahlenschutz in der Medizin
Strahlenschutzkommission
Die jährlichen Veröffentlichungen werden in Jahresberichten zusammengefasst. Diese sind auf www.ssk.de unter dem Menüpunkt "Publikationen" abrufbar.
International Commission on Radiological Protection (ICRP)
Die International Commission on Radiological Protection (ICRP) befasst sich mit dem Schutz von Mensch und Umwelt vor den Wirkungen ionisierender Strahlung. Ihr Sitz ist in Ottawa in Kanada. Publikationen der ICRP und weitere Informationen können auf der Internetseite der ICRP eingesehen werden: www.icrp.org.
Bundesministerium des Innern (BMI)
Gesetz zum Schutz vor der schädlichen Wirkung ionisierender Strahlung (Strahlenschutzgesetz, StrlSchG). Bundesgesetzblatt. 2017: Teil I Nr. 42. Internet: www.gesetze-im-internet.de/strlschg
Fachliteratur
Balermpas P, Rödel F, Rödel C, Krause M, Linge A, Lohaus F, Baumann M, Tinhofer I, Budach V, Gkika E, Stuschke M, Avlar M, Grosu AL, Abdollahi A, Debus J, Bayer C, Stangl S, Belka C, Pigorsch S, Multhoff G, Combs SE, Mönnich D, Zips D, Fokas E. CD8+ tumour-infiltrating lymphocytes in relation to HPV status and clinical outcome in patients with head and neck cancer after postoperative chemoradiotherapy: A multicentre study of the German cancer consortium radiation oncology group (DKTK-ROG). Int J Cancer 2016; 138(1):171-181. DOI: 10.1002/ijc.29683.
Baumann BC, Zeng C, Freedman GM, Verginadis II, MacArthur KM, Lin LL, Vachani C, Koumenis C, Solberg TD, Metz JM. Avoiding antiperspirants during breast radiation therapy: Myth or sound advice? Radiother Oncol 2017; 124(2):204-207. DOI: 10.1016/j.radonc.2017.06.021.
Baumann M, Krause M, Overgaard J, Debus J, Bentzen SM, Daartz J, Richter C, Zips D, Bortfeld T. Radiation oncology in the era of precision medicine. Nature Reviews Cancer 2016; 16(4): 234-249. DOI: http://dx.doi.org/10.1038/nrc.2016.18.
Baumann M, Overgaard J. Bridging the valley of death: The new Radiotherapy & Oncology section "First in man - Translational innovations in radiation oncology." Radiotherapy and Oncology 2016; 118(2): 217-219. DOI: http://dx.doi.org/10.1016/j.radonc.2016.02.005.
Blanchet MR, Israël-Assayag E, Cormier Y. Inhibitory Effect of Nicotine on Experimental Hypersensitivity Pneumonitis In Vivo and In Vitro. American Journal of Respiratory and Critical Care Medicine, 2004; 169(8): 903-909. DOI: 10.1164/rccm.200210-1154OC.
Bostel T, Nicolay N.H, Grossmann G, Mohr A, Delorme S, Echner G, Häring P, Pfaffenberger A, Debus J, Sterzing F. MR-Guidance – eine klinische Studie zur Evaluation einer shuttlebasierten, MRT-geführten Radiotherapie. Strahlenther Onkol 2014; 190 (1S): 1-164.
Bostel, T, Pfaffenberger A, Delorme S et al. Prospective feasibility analysis of a novel off-line approach for MR-guided radiotherapy. Strahlenther Onkol (2018) 194: 425. doi.org/10.1007/s00066-017-1258-y
Carolan M, Dao P, Fox C, Metcalfe P. Effect of hip prostheses on radiotherapy dose. Journal of Medical Imaging and Radiation Oncology 2000; 44(3): 290-295. DOI: 10.1046/j.1440-1673.2000.00816.x.
Coppes R, Dubrovska A. Targeting stem cells in radiation oncology. Clinical Oncology 2017; 29(6), 329-334. DOI: http://dx.doi.org/10.1016/j.clon.2017.03.005.
Dörffel W, Riepenhausen M, Lüders H, Brämswig J, Schellong G. Sekundäre maligne Neoplasien nach Therapie eines Hodgkin-Lymphoms im Kindes- und Jugendalter. Eine Kohortenstudie mit mehr als 30 Jahren Nachbeobachtung. Dtsch Arztebl Int 2015; 112(18): 320–327. DOI: 10.3238/arztebl.2015.0320.
Fiebich M, Zink K. Strahlenbelastung in der Schwangerschaft. Onkologe 2018; 24: 545-551. DOI: doi.org/10.1007/s00761-018-0367-2.
Gauter-Fleckenstein B, Isreal CW, Dorenkamp M et al. DEGRO/DGK guideline for radiotherapy in patients with cardiac implantable electronic devices. Strahlenther Onkol 2015; 191:393–404. DOI: 10.1007/s00066-015-0817-3.
Goretzki G. Medizinische Strahlenkunde. Physikalisch-technische Grundlagen. 2. Auflage. München: Elsevier; 2004.
Kassenärztliche Bundesvereinigung. Vereinbarung von Qualifikationsvoraussetzungen gemäß § 135 Abs. 2 SGB V zur Durchführung von Untersuchungen in der diagnostischen Radiologie und Nuklearmedizin und von Strahlentherapie (Vereinbarung zur Strahlendiagnostik und -therapie). Anlage zum Bundesmantelvertrag für Ärzte. 2015.
Linge A, Löck S, Gudziol V, Nowak A, Lohaus F, von Neubeck C, Jütz M, Abdollahi A, Debus J, Tinhofer I, Budach V, Sak A, Stuschke M, Balermpas P, Rödel C, Avlar M, Grosu AL, Bayer C, Belka C, Pigorsch S, Combs SE, Welz S, Zips D, Buchholz F, Aust DE, Baretton GB, Thames HD, Dubrovska A, Alsner J, Overgaard J, Baumann M, Krause M; DKTK-ROG. Low Cancer Stem Cell Marker Expression and Low Hypoxia Identify Good Prognosis Subgroups in HPV(-) HNSCC after Postoperative Radiochemotherapy: A Multicenter Study of the DKTK-ROG. Clin Cancer Res 2016; 22(11):2639-2649. DOI: 10.1158/1078-0432.CCR-15-1990.
Linge A, Löck S, Krenn C, Appold S, Lohaus F, Nowak A, Gudziol V, Baretton GB, Buchholz F, Baumann M, Krause M. Independent validation of the prognostic value of cancer stem cell marker expression and hypoxia-induced gene expression for patients with locally advanced HNSCC after postoperative radiotherapy. Clinical and Translational Radiation Oncology 2016; 1:19-26. DOI: http://dx.doi.org/10.1016/j.ctro.2016.10.002.
Löck S, Perrin R, Seidlitz A, Bandurska-Luque A, Zschaeck S, Zöphel K, Krause M, Steinbach J, Kotzerke J, Zips D, Troost EGC, Baumann M. Residual tumour hypoxia in head-and-neck cancer patients undergoing primary radiochemotherapy, final results of a prospective trial on repeat FMISO-PET imaging. Radiother Oncol 2017; pii: S0167-8140(17)32517-3. DOI: 10.1016/j.radonc.2017.08.010.
Margulies A et al. [Hrsg.] Onkologische Krankenpflege. 5. Auflage. Berlin, Heidelberg: Springer; 2011.
Maurer J, Schäfer C, Maurer O, Kölbl O. Angst und Depressivität bei Tumorpatienten im Verlauf der radioonkologischen Behandlung. Strahlentherapie und Onkologie 2012; 188(10): 940–945.
Mittauer K, Paliwal B, Hill P, et al. A New Era of Image Guidance with Magnetic Resonance-guided Radiation Therapy for Abdominal and Thoracic Malignancies. Muacevic A, Adler JR, eds. Cureus. 2018;10(4):e2422. doi:10.7759/cureus.2422.
Pilz K, Hoffmann AL, Baumann M, Troost EGC. Vertebral fractures – An underestimated side-effect in patients treated with radio(chemo)therapy. Radiotherapy and Oncology 2016; 118(3): 421-423. DOI: http://dx.doi.org/10.1016/j.radonc.2016.02.021.
Reif K, de Vries U. Wege aus der Erschöpfung. Ratgeber zur tumorbedingten Fatigue. Bern: Hans Huber; 2011.
Reiser M, Kuhn FP, Debus J. Duale Reihe: Radiologie. 3. Auflage. Stuttgart: Thieme; 2011.
Schicha H, Schober O. Nuklearmedizin. Basiswissen und klinische Anwendung. 5. Auflage. Stuttgart, New York: Schattauer; 2003.
Sterzing F, Kratochwil C, Fiedler H, Katayama S, Habl G, Kopka K, Afshar-Oromieh A, Debus J, Haberkorn U, Giesel FL. (68)Ga-PSMA-11 PET/CT: a new technique with high potential for the radiotherapeutic management of prostate cancer patients. Eur J Nucl Med Mol Imaging 2016; 43(1):34-41. DOI: 10.1007/s00259-015-3188-1.
Stöver I, Feyer P. Praxismanual Strahlentherapie. Berlin, Heidelberg: Springer; 2010.
Taylor C, Correa C, Duane FK, Aznar MC, Anderson SJ, Bergh J, Dodwell D, Ewertz M, Gray R, Jagsi R, Pierce L, Pritchard KI, Swain S, Wang Z, Wang Y, Whelan T, Peto R, McGale P; Early Breast Cancer Trialists' Collaborative Group. Estimating the Risks of Breast Cancer Radiotherapy: Evidence From Modern Radiation Doses to the Lungs and Heart and From Previous Randomized Trials. J Clin Oncol 2017; 35(15):1641-1649. DOI: 10.1200/JCO.2016.72.0722.
Tinhofer I, Budach V, Saki M, Konschak R, Niehr F, Jöhrens K, Weichert W, Linge A, Lohaus F, Krause M, Neumann K, Endris V, Sak A, Stuschke M, Balermpas P,Rödel C, Avlar M, Grosu AL, Abdollahi A, Debus J, Belka C, Pigorsch S, Combs SE, Mönnich D, Zips D, Baumann M; DKTK-ROG. Targeted next-generation sequencing of locally advanced squamous cell carcinomas of the head and neck reveals druggable targets for improving adjuvant chemoradiation. Eur J Cancer 2016;57:78-86. DOI: 10.1016/j.ejca.2016.01.003.
van der Est H, Prins P, Heijmen BJ, Dirkx ML. Intensity modulated radiation therapy planning for patients with a metal hip prosthesis based on class solutions. Pract Radiat Oncol 2012; 2(1): 35-40. DOI: 10.1016/j.prro.2011.04.006.
Weytjens R, Erven K, De Ruysscher D. Radiation pneumonitis: occurrence, prediction, prevention and treatment. Belg J Med Oncol 2013; 7(4): 105-110.
Wijsman R, Dankers F, Troost EGC, Hoffmann AL, van der Heijden EHFM, de Geus-Oei LF, Bussink J. Comparison of toxicity and outcome in advanced stage non-small cell lung cancer patients treated with intensity-modulated (chemo-)radiotherapy using IMRT or VMAT. Radiotherapy and Oncology 2017; 122(2), 295. DOI: http://dx.doi.org/10.1016/j.radonc.2016.11.015.
Zindler JD, Jochems A, Lagerwaard FJ, Beumer R, Troost EGC, Eekers DBP, Compter I, van der Toorn PP, Essers M, Oei B, Hurkmans CW, Bruynzeel AME, Bosmans G, Swinnen A, Leijenaar RTH, Lambin P. Individualized early death and long-term survival prediction after stereotactic radiosurgery for brain metastases of non-small cell lung cancer: Two externally validated nomograms. Radiotherapy and Oncology 2017; 123(2), 189-194. DOI: http://dx.doi.org/10.1016/j.radonc.2017.02.006.
Zwicker F, Swartman B, Roeder F, Sterzing F, Hauswald H, Thieke C, Weber KJ, Huber PE, Schubert K, Debus J, Herfarth K. In vivo measurement of dose distribution in patients' lymphocytes: helical tomotherapy versus step-and-shoot IMRT in prostate cancer. J Radiat Res 2015; 56(2):239-47. DOI: 10.1093/jrr/rru096.