Immunvermittelte Nebenwirkungen häufiger bei bestehender Autoimmunerkrankung?
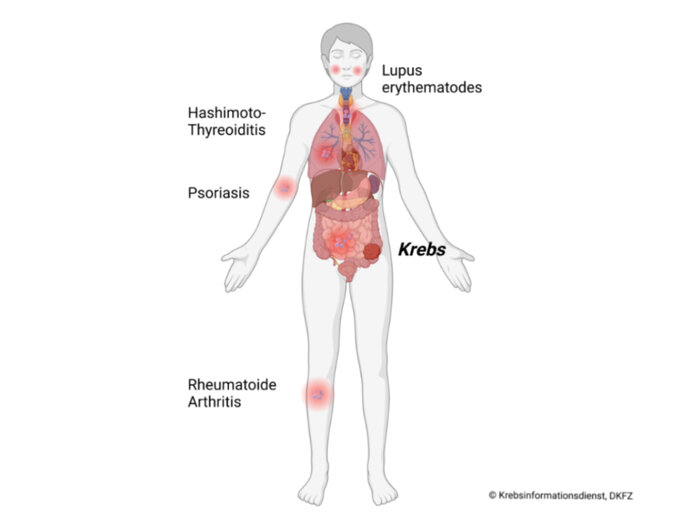
Bild: Krebsinformationsdienst, DKFZ, erstellt mit BioRender.com
Die bisherigen, allerdings häufig kleinen und retrospektiven Studien deuten darauf hin: Krebsbetroffene, die bereits vor Therapiebeginn eine Autoimmunerkrankung hatten, bekommen unter Immun-Checkpoint-Hemmern etwas häufiger immunvermittelte Nebenwirkungen. Diese sogenannten irAEs (immune-related adverse events) sind entweder
- ein "Aufflackern" (Flare) der bereits bestehenden Erkrankung
- oder auch eine neu auftretende Autoimmunreaktion.
Je nach Studie traten Flares der Autoimmunerkrankung unterschiedlich häufig auf: Sie betrafen in Studien etwa zwischen 1 und 70 Prozent der Teilnehmenden. Die große Mehrheit der auftretenden Flares und irAEs wird in den bisherigen Untersuchungen zum Thema als mild und gut behandelbar beschrieben. In einzelnen Fällen kam es aber auch zu schweren Verläufen.
Cave Patienten-Auswahl: Man muss bei der Interpretation der bisherigen Daten davon ausgehen, dass hier eine Selektion von Patienten stattgefunden hat. Sehr wahrscheinlich wurden bevorzugt Patientinnen und Patienten behandelt, bei denen die behandelnden Ärzte weniger bedrohliche Komplikationen befürchtet und/oder einen hohen Nutzen der Behandlung angenommen haben.
Es gibt inzwischen aber erste, in der Regel kleine Auswertungen auch zur Behandlung von Betroffenen mit potenziell lebensbedrohlichen Autoimmunerkrankungen wie einer Myasthenia gravis oder entzündlichen Autoimmunerkrankungen des Darmtraktes.
irAEs: mögliche Einflussfaktoren
Ob Flares oder immunvermittelte Nebenwirkungen auftreten, hängt grundsätzlich davon ab,
- an welcher Krebserkrankung Betroffene erkrankt sind,
- an welcher Autoimmunerkrankung sie leiden und/oder
- mit welchen Checkpoint-Inhibitoren sie behandelt werden.
Zur Krebsart: Die meisten Untersuchungen zur Rolle vorbestehender Autoimmunerkrankungen gibt es beim malignen Melanom und bei Lungenkrebs. In anderen Studien sind häufig Betroffene mit verschiedenen, zum Teil selteneren Krebserkrankungen wie zum Beispiel Kopf-Hals-Tumoren oder urologischen Tumoren zusammengefasst.
In der Regel reicht hier jedoch die Fallzahl nicht für separate Untergruppenanalysen einzelner Krebsarten aus. Für Krebserkrankungen wie den triple-negativen Brustkrebs, bei denen Checkpoint-Hemmer erst seit kurzer Zeit eingesetzt werden, sind bisher keine systematischen Untersuchungen zum Thema erschienen.
Zur Art der Immunerkrankung: Flares wurden beispielsweise besonders häufig beschrieben bei Krebspatienten mit rheumatoiden Autoimmunerkrankungen beziehungsweise Psoriasis.
Zur eingesetzten Immuntherapie: Einige Auswertungen gibt es zu der Frage, ob die Art beziehungsweise das Ziel-Eiweiß des Checkpoint-Hemmers die Häufigkeit und Schwere von Flares oder neu auftretenden irAEs bei Patienten mit vorbestehenden Autoimmunerkrankungen beziehungsweise immunvermittelten Erkrankungen beeinflusst.
Die Vermutung liegt nahe, weil sich zum einen ein Funktionsverlust von CTLA-4 oder PD-1/PD-L1 im Tiermodell unterschiedlich auswirkt. Zum anderen ist bekannt, dass sich die Nebenwirkungsspektren von CTLA-4-Blockern wie Ipilimumab und PD-1- und PD-L1-Blockern wie Nivolumab, Pembrolizumab oder Atezolizumab auch bei Patienten ohne Autoimmunerkrankungen deutlich unterscheiden. Ein prominentes Beispiel ist der Darmtrakt. Er ist unter CTLA-4-Hemmern wesentlich häufiger von irAEs betroffen als unter PD-1-/PD-L1-Hemmern.
In ersten Studien zeigte sich beispielsweise, dass nicht jeder Krebspatient mit vorbestehender immunvermittelter entzündlicher Erkrankung des Darms unter CTLA-4-Hemmern einen Flare bekommt. In einer Studie war der Einsatz eines CTLA-4-Hemmers bei Patientinnen und Patienten mit vorbestehenden immunvermittelten entzündlichen Erkrankungen des Darms kein unabhängiger Einflussfaktor für gastrointestinale Nebenwirkungen.
Insgesamt gibt es zu dieser Fragestellung bisher aber noch wenige aussagekräftige Daten.
Flare – wirklich durch die Immuntherapie?
Grundsätzlich muss man bei der Interpretation der präsentierten Daten beachten: Es ist nicht immer einfach zu entscheiden, ob es sich bei unter der Therapie auftretenden irAEs um einen Flare der vorbestehenden immunvermittelten Erkrankung handelt oder um ein unabhängiges, neues Ereignis – beispielsweise, wenn Patienten mit Mobus Crohn oder Colitis ulcerosa mit Ipilimumab behandelt werden. Hinzu kommt, dass nicht mit Sicherheit gesagt werden kann, dass ein Flare einer Autoimmunerkrankung durch die Checkpoint-Hemmer-Behandlung ausgelöst wurde und nicht ohnehin aufgetreten wäre.
Ein Beispiel: In einer Studie zur Behandlung von Patienten mit vorbestehenden chronisch-entzündlichen Darmerkrankungen (IBD) hatten die Patienten mit IBD, die mit Checkpoint-Hemmern behandelt wurden, erheblich mehr gastrointestinale unerwünschte Ereignisse als Patienten ohne IBD unter vergleichbarer Therapie: 41 versus 11 Prozent. Hier fehlt aber der Vergleich mit (Krebs-)Patienten mit IBD, die keine Checkpoint-Hemmer erhalten.
Was weiß man zur Wirksamkeit?
Inzwischen geht man davon aus, dass eine Immuntherapie mit Checkpoint-Hemmern bei Patientinnen und Patienten mit vorbestehenden Autoimmunerkrankungen insgesamt ähnlich gut wirkt wie bei anderen Krebspatienten.
In einer aktuellen, großen retrospektiven Analyse wurde die Mortalität von Krebspatientinnen und -patienten unter PD-1-/PD-L1-Hemmer-Behandlung mit vorbestehender Autoimmunerkrankung untersucht. Verglichen wurden 17.497 Krebspatienten mit vorbestehender Autoimmunerkrankung und 17.497 gematchte Patienten ohne eine solche.
In dieser Analyse hatten die Patienten mit Autoimmunerkrankungen eine vergleichbare Prognose wie die Patienten in der Kontrollgruppe. Bei Patienten mit Hashimoto-Thyreoiditis oder Vitiligo in der Vorgeschichte war die Mortalität sogar statistisch signifikant vermindert.
Immunsuppressiva zu Beginn der Immuntherapie: ungünstig?
Eine schwer zu interpretierende Gruppe stellen die Patientinnen und Patienten dar, die bereits zu Beginn einer Therapie mit Checkpoint-Hemmern wegen ihrer Autoimmunerkrankung unter immunsuppressiver Behandlung stehen.
Allein die Tatsache, dass sie diese Behandlung derzeit benötigen, kann auf eine aktive beziehungsweise aggressiv verlaufende Autoimmunerkrankung hindeuten. Auf der anderen Seite kann die Immunsuppression wiederum das Auftreten von Flares und weiteren immunvermittelten Nebenwirkungen verhindern oder zumindest vermindern.
Hinweise auf schlechtere Prognose unter Kortikosteroiden: Für diese Gruppe gibt es tatsächlich Hinweise aus einzelnen Studien darauf, dass die Prognose der Betroffenen unter einer Immuntherapie insgesamt etwas schlechter sein könnte als die von Patientinnen und Patienten, die zu Beginn einer Therapie mit Checkpoint-Hemmern keine immunsupprimierenden Medikamente erhalten. In diesen Studien wurde das insbesondere für eine Immununterdrückung mit Kortikosteroiden beobachtet.
In einer Studie zu Melanompatienten mit vorbestehenden Autoimmunerkrankungen unter Ipilimumab-PD-1-Hemmer-Kombinationstherapien hatte beispielsweise eine Immunsuppression mit Kortikosteroiden zu Behandlungsbeginn einen ungünstigen Einfluss auf das Gesamtüberleben. Hierzu ist aber noch mehr Forschung notwendig. Ein wichtiger Aspekt ist hier, ob gezieltere Formen der Immununterdrückung möglicherweise einen geringeren Einfluss haben als die sehr "breit" wirkenden Kortikosteroide.
Wie geht es weiter?
Die bisherigen Untersuchungen zum Thema deuten darauf hin, dass viele Krebspatienten mit vorbestehenden immunvermittelten Erkrankungen sehr wahrscheinlich ebenso von Immun-Checkpoint-Hemmern profitieren wie Patienten ohne solche Erkrankungen. Daher laufen inzwischen erste prospektive klinische Studien, in die spezifisch Krebspatienten mit Autoimmunerkrankungen aufgenommen und mit Checkpoint-Hemmern behandelt werden. Diese Studien werden in den nächsten Jahren helfen, das optimale Management solcher Patienten besser zu definieren.
Fazit
Die bisherigen Daten zeigen, dass eine Autoimmunerkrankung oder eine immunvermittelte entzündliche Erkrankung (IMID) in der Vorgeschichte nicht automatisch eine Kontraindikation für eine Behandlung mit Checkpoint-Hemmern darstellt – insbesondere, wenn die Erkrankung gut unter Kontrolle ist, keine gleichwertigen Alternativen zur Verfügung stehen und keine lebensbedrohlichen Konsequenzen zu befürchten sind.
Bezüglich der Behandlung von Krebsbetroffenen mit vorbestehenden Autoimmunerkrankungen oder IMIDs mit Immun-Checkpoint-Hemmern sind aber noch Fragen offen. Dazu gehört beispielsweise die Frage, welche Patientinnen und Patienten besonders gefährdet für einen schweren Flare oder irAEs sind, oder auch die Fragen, mit welchen Medikamenten Autoimmun-Flares und irAEs am besten vorgebeugt werden kann oder wie sie behandelt werden sollten.
Ergebnisse laufender klinischer Studien werden in den nächsten Jahren dabei helfen, den möglichen Schaden und Nutzen genauer zu definieren.
Zum Weiterlesen: Verwendete Quellen und vertiefende Informationen
Übersichtsarbeiten und Fachveröffentlichungen
Abdel-Wahab N, Shah M, Lopez-Olivo MA, Suarez-Almazor ME. Use of Immune Checkpoint Inhibitors in the Treatment of Patients With Cancer and Preexisting Autoimmune Disease. Ann Intern Med. 2018 Jul 17;169(2):133-134. doi: 10.7326/L18-0209.
Alexander S, Swami U, Kaur A, Gao Y, Fatima M, Ginn MM, Stein JE, Grivas P, Zakharia Y, Singh N. Safety of immune checkpoint inhibitors in patients with cancer and pre-existing autoimmune disease. Ann Transl Med. 2021 Jun;9(12):1033. doi: 10.21037/atm-20-8124.
Calvo V, Fernández MA, Collazo-Lorduy A, Franco F, Núñez B, Provencio M. Use of immune checkpoint inhibitors in patients with solid tumors and pre-existing autoimmune or inflammatory disease: real-world data. Lung Cancer Manag. 2021 Jul 2;10(4):LMT51. doi: 10.2217/lmt-2021-0003.
Fountzilas E, Lampaki S, Koliou GA, Koumarianou A, Levva S, Vagionas A, Christopoulou A, Laloysis A, Psyrri A, Binas I et al. Real-world safety and efficacy data of immunotherapy in patients with cancer and autoimmune disease: the experience of the Hellenic Cooperative Oncology Group. Cancer Immunol Immunother. 2022 Feb;71(2):327-337. doi: 10.1007/s00262-021-02985-6.
Kehl KL, Yang S, Awad MM, Palmer N, Kohane IS, Schrag D. Pre-existing autoimmune disease and the risk of immune-related adverse events among patients receiving checkpoint inhibitors for cancer. Cancer Immunol Immunother. 2019 Jun;68(6):917-926. doi: 10.1007/s00262-019-02321-z.
Kennedy LC, Bhatia S, Thompson JA, Grivas P. Preexisting Autoimmune Disease: Implications for Immune Checkpoint Inhibitor Therapy in Solid Tumors. J Natl Compr Canc Netw. 2019 Jun 1;17(6):750-757. doi: 10.6004/jnccn.2019.7310.
Meserve J, Facciorusso A, Holmer AK, Annese V, Sandborn WJ, Singh S. Systematic review with meta-analysis: safety and tolerability of immune checkpoint inhibitors in patients with pre-existing inflammatory bowel diseases. Aliment Pharmacol Ther. 2021 Feb;53(3):374-382. doi: 10.1111/apt.16217.
Tang H, Zhou J, Bai C. The Efficacy and Safety of Immune Checkpoint Inhibitors in Patients With Cancer and Preexisting Autoimmune Disease. Front Oncol. 2021 Feb 22;11:625872. doi: 10.3389/fonc.2021.625872.
Tang K, Tiu BC, Wan G, Zhang S, Nguyen N, Leung B, Gusev A, Reynolds KL, Kwatra SG, Semenov YR. Pre-Existing Autoimmune Disease and Mortality in Patients Treated With Anti-PD-1 and Anti-PD-L1 Therapy. J Natl Cancer Inst. 2022 Feb 21:djac046. doi: 10.1093/jnci/djac046.
Tison A, Quéré G, Misery L, Funck-Brentano E, Danlos FX, Routier E, Robert C, Loriot Y, Lambotte O, Bonniaud B et al., Groupe de Cancérologie Cutanée, Groupe Français de Pneumo-Cancérologie, and Club Rhumatismes et Inflammations. Safety and Efficacy of Immune Checkpoint Inhibitors in Patients With Cancer and Preexisting Autoimmune Disease: A Nationwide, Multicenter Cohort Study. Arthritis Rheumatol. 2019 Dec;71(12):2100-2111. doi: 10.1002/art.41068.
Wu C, Zhong L, Wu Q, Lin S, Xie X. The safety and efficacy of immune-checkpoint inhibitors in patients with cancer and pre-existing autoimmune diseases. Immunotherapy. 2021 Apr;13(6):527-539. doi: 10.2217/imt-2020-0230.
Yamaguchi A, Saito Y, Okamoto K, Narumi K, Furugen A, Takekuma Y, Sugawara M, Kobayashi M. Preexisting autoimmune disease is a risk factor for immune-related adverse events: a meta-analysis. Support Care Cancer. 2021 Dec;29(12):7747-7753. doi: 10.1007/s00520-021-06359-7.
Zhang K, Kong X, Li Y, Wang Z, Zhang L, Xuan L. PD-1/PD-L1 Inhibitors in Patients With Preexisting Autoimmune Diseases. Front Pharmacol. 2022 Mar 18;13:854967. doi: 10.3389/fphar.2022.854967.